题目内容
【题目】t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示. 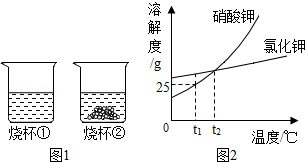
(1)烧杯②种的上层清液是否达到饱和状态?(填“是”“否”或“无法判断”);
(2)烧杯①中溶解的溶质是(写名称或化学式);
(3)将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水g;
(4)关于图1中烧杯内的物质,下列说法正确的是 .
A.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
B.蒸发一定量的水,两烧杯中都一定有固体析出
C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)
【答案】
(1)是
(2)氯化钾
(3)50
(4)AD
【解析】解:(1)烧杯②中有固体剩余,所以上层的清液达到饱和状态;(2)t1℃时,氯化钾的溶解度大于硝酸钾的溶解度,剩余烧杯①中溶解的溶质是氯化钾;(3)t1℃时硝酸钾的溶解度是25g,所以饱和溶液的溶质质量分数为: ![]() ×100%=20%,所以将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水
×100%=20%,所以将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水 ![]() ﹣50g=50g;(4)A、等质量的固体溶解在100g水中,烧杯①中没有固体剩余,烧杯②中有固体剩余,所以烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数,故A正确; B、烧杯①中溶液的状态不能确定,所以蒸发一定量的水,两烧杯中不一定有固体析出,故B错误;
﹣50g=50g;(4)A、等质量的固体溶解在100g水中,烧杯①中没有固体剩余,烧杯②中有固体剩余,所以烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数,故A正确; B、烧杯①中溶液的状态不能确定,所以蒸发一定量的水,两烧杯中不一定有固体析出,故B错误;
C、将两个烧杯中的溶液混合,充分搅拌后,烧杯中不一定还有剩余固体,故C错误
D、t2时两种物质的溶解度相等,升温到t2时,两种物质都完全溶解形成不饱和溶液,溶质和溶液质量都相等,质量分数相等,故D正确.
故选:AD.
故答案为:(1)是;(2)氯化钾;(3)50;(4)AD.
根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案