题目内容
【题目】下列四个图象,分别对应四种操作过程,其中正确的是
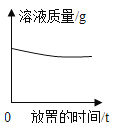
A. 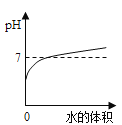 向盐酸中不断加水
向盐酸中不断加水
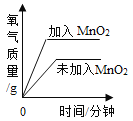
B. 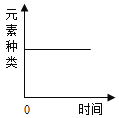 一定质量的镁在密闭的容器内燃烧
一定质量的镁在密闭的容器内燃烧
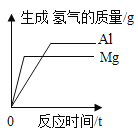
C. 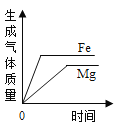 等质量的铁和镁同时分别放入两份溶质质量分数相同的足量稀盐酸中
等质量的铁和镁同时分别放入两份溶质质量分数相同的足量稀盐酸中
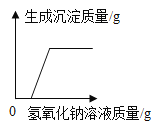
D. 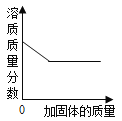 某温度下,向一定质量的饱和氯化钠溶液中加入氯化钠固体
某温度下,向一定质量的饱和氯化钠溶液中加入氯化钠固体
【答案】B
【解析】
向盐酸中不断加水,酸性逐渐减弱,PH无穷尽的接近于7,但不会等于或超过7,所以A图象描述不正确;一定质量的镁在密闭的容器内燃烧,根据质量守恒定律,元素的种类是不变的,所以B图象表达正确;由于镁的活泼比铁的强,所以等质量的铁和镁同时分别放入两份溶质质量分数相同的足量稀盐酸镁用的时间短,由公式:m(H2)=(金属的化合价/金属的相对原子质量)×金属的质量,所以镁产生的氢气多,所图象以C描述错误;在某温度下,向一定质量的饱和氯化钠溶液中加入氯化钠固体,由于是饱和溶液,不能继续溶解溶质了,所以原溶液中溶质的质量分数不变,故D表达不正确。

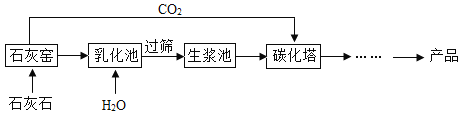
【题目】小强在帮老师整理实验室时,发现一瓶未密封的KOH固体,对其成分提出以下假设;并在老师的指导下进行试验探究。
(查阅资料):①KOH与NaOH的化学性质相似;请用化学方程式解释KOH变质的原因:_____.
②K2CO3溶液呈碱性,BaCl2溶液、KCl溶液呈中性;
(猜想与假设)通过分析,提出如下猜想:
假设Ⅰ:只含KOH; 假设Ⅱ:含KOH和K2CO3; 假设Ⅲ:只含K2CO3:
(实验探究)
实验操作步骤 | 实验现象 | 实验结论 |
①取少量样品于试管中,加入足量的稀盐酸 | 有气泡产生 | 假设_____不正确 |
②另取少量样品于试管中,加水溶解,加入过量的BaCl2溶液,振荡,静置 | 有白色沉淀生成 | 假设Ⅲ正确 |
③取②中上层清液,滴加无色酚酞溶液 | _____ |
(问题讨论)步骤②中加入过量BaCl2溶液的作用是_____。
(拓展应用)完全变质的KOH也有利用价值,从K2CO3组成或性质看,其在农业上的用途是_____。