题目内容
某化学兴趣小组的同学在实验室配制质量分数为20%的碳酸钠溶液,并完成有关实验。
(1)配制100g质量分数为20%的碳酸钠溶液。
①配制方法A、需要碳酸钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。配制方法B、若用40%的碳酸钠溶液稀释成100克20%碳酸钠溶液,则需取40%的碳酸钠溶液多少亳升?(密度为1.4克/毫升) (填答案)。
②配制溶质质量分数一定的碳酸钠溶液常按以下操作顺序进行。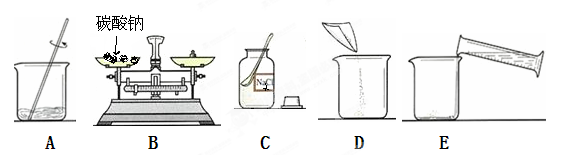
则用上图所示的序号表示正确配制该溶液的操作顺序为 。
③用托盘天平称量所需的碳酸钠时,发现托盘天平的指针偏向左盘,应 。
A.增加适量固体 B.减少适量固体
C.调节游码 D.添加砝码
④分析:以下原因可能导致配到的碳酸钠溶液溶质质量分数小于8%的是( )
A、固体中混有杂质
B、量水时仰视读数
C、配好后装入试剂瓶中时有少量液体洒出
D、量水时俯视读数
(2)取上述配制得到的20%的碳酸钠溶液53克,加入68.4克某浓度的稀盐酸后,恰好完全反应,求反应后所得溶液的溶质质量分数。
(1)①20; 80; 35.7;②CBDEA;③B;④AB ;(2)10%。
解析试题分析:(1)①配制方法A、需要碳酸钠固体的质量为100g×20%=20g,水的体积为100-20=80mL;配制方法B,设需要40%的碳酸钠溶液为xml
X×40%×1.4g/mi=100×20% X=35.7ml②配制溶质质量分数一定的碳酸钠溶液常按以下操作顺序进行用上图所示的序号表示正确配制该溶液的操作顺序为CBDEA;③用托盘天平称量所需的碳酸钠时,发现托盘天平的指针偏向左盘,应减少固体;④分析:以下原因可能导致配到的碳酸钠溶液溶质质量分数小于8%的是A、固体中混有杂质; B、量水时仰视读数 ; (2)取上述配制得到的20%的碳酸钠溶液53克,加入68.4克某浓度的稀盐酸后,恰好完全反应,求反应后所得溶液的溶质质量分数
设反应后所得溶液中溶质质量为X,生成二氧化碳的质量为Y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
117 44
20%×53g X y
106:117=20%×53g:X 106:44=20%×53g:y
X=11.7g y=4.4g
反应后溶液的质量为:53g+63.4g-4.4g=112g
反应后溶液的溶质质量分数为: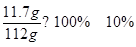
考点:配制溶液及根据化学方程式的计算

一种抗生素为粉末状固体,每瓶含0.5g,注射时应配成质量分数为20%的溶液,则使用时每瓶至少需加入蒸馏水
| A.1mL | B.2mL | C.3mL | D.4mL |
质量法是化学实验中测定物质组成时常用的一种方法。现有11 g气体,经测含碳元素3g,其余都是氧元素。下列有关说法正确的是
| A.气体可能是CO2和O2的混合物 |
| B.气体可能是CO和CO2的混合物 |
| C.气体组成有4种情况 |
| D.若气体由三物质组成,则三物质质量比可能是7:3:4 |