题目内容
【题目】多彩的“碳”,多姿的生活,碳及其化合物在生活中应用广泛。
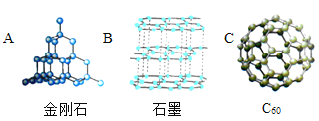
(1)碳的单质有多种,具有下列结构的碳单质中,由分子构成的是(填序号)______。
(2)将两只用于医学研究的小白鼠分别放入盛放CO、CO2的两个瓶中,拧紧瓶盖,结果两只小白鼠很快都死了,造成小白鼠死亡的主要原因_______(填“相同”或“不同”)。
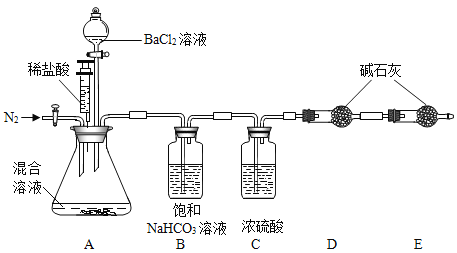
(3)如图是教材中关于二氧化碳性质的实验探究。
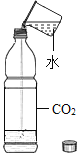
①此实验探究的目的是____,能证明此性质的实验现象是____。
②CO2溶于水后是否发生了化学变化?______(填“是”或“否”)你怎样用实验来证明?________(简述实验操作过程与现象)
【答案】C 不同 探究二氧化碳的溶解性 塑料瓶变瘪 是 往CO2溶于水后的溶液中滴加紫色石蕊试液,紫色石蕊试液变红色
【解析】
(1)金刚石和石墨是由碳原子构成的,而C60是由分子构成的;
故填:C;
(2)二氧化碳,不能帮助呼吸,本身无毒,小白鼠窒息而死;而一氧化碳,是有毒的气体,小白鼠中毒而死,故造成小白鼠死亡的原因不同。
故填:不同;
(3)①往盛有二氧化碳的矿泉水瓶中倾倒水,二氧化碳被水溶解,瓶内气体的压强变小,瓶子变瘪,说明二氧化碳减少了,CO2能溶于水;
故填:探究二氧化碳的溶解性;塑料瓶变瘪;
②往CO2溶于水后的溶液中滴加紫色石蕊试液,紫色石蕊试液变红色,说明二氧化碳和水反应生成碳酸,且碳酸能使紫色石蕊试液变红色;
故填:是;往CO2溶于水后的溶液中滴加紫色石蕊试液,紫色石蕊试液变红色。

【题目】下面是同学们测定黄铜(铜锌合金)中铜的质量分数的过程。
(1)小华同学取10g黄铜,加入足量的稀硫酸,共收集到气体0.2g,则黄铜中铜的质量分数是多少?____________________(写出计算过程)
(2)小婷同学另取10g黄铜于烧杯中,向烧杯中加入稀硫酸,测得加入的稀硫酸质量和烧杯中剩余物的质量如下表:
加入稀硫酸的质量/g | 30 | 60 | 90 | 120 |
烧杯中剩余物的质量/g | 39.94 | m | 99.82 | 129.8 |
①表中m=____________,从表中的数据分析,当小婷同学加入_________g稀硫酸时,烧杯中刚好没有气泡产生。
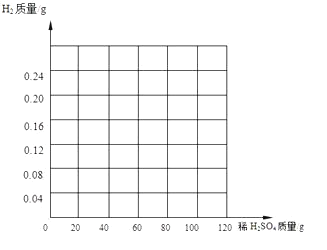
②请在下图画出10g黄铜加入稀硫酸与生成氢气的质量的图像____________________。