题目内容
【题目】焦亚硫酸钠(Na2S2O5)是一种常用的食品抗氧化剂,小金模仿化工生产,用如图装置来制取Na2S2O5:
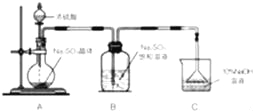
已知:A中发生的反应为:H2SO4(浓)+Na2SO3═Na2SO4+SO2↑+H2O
B中发生的反应为:Na2SO3+SO2═Na2S2O5
(1)图中盛放浓硫酸的仪器名称是 。
(2)写出C中发生反应的化学方程式 。
(3)在实验过程中,滴加浓硫酸不宜过快,理由是 。
(4)该实验开始滴加浓硫酸时,应先除尽装置内的空气,若忘记这一操作,新制取的Na2S2O5产品中会混有Na2SO4杂质,这与O2的 有关(填化学性质)。
【答案】
(1)分液漏斗
(2)SO2+2NaOH═Na2SO3+H2O
(3)防止生成二氧化硫气体过快,来不及与B中的亚硫酸钠进一步反应生成Na2S2O5
(4)氧化性
【解析】
试题分析:
(1)图中盛放浓硫酸的仪器的名称为分液漏斗;故填分液漏斗;
(2)反应过程中产生有害气体二氧化硫,需要进行尾气处理,二氧化硫与二氧化碳性质相似,与氢氧化钠反应生成相应的盐和水;反应的化学方程式为:SO2+2NaOH═Na2SO3+H2O;故填:SO2+2NaOH ═Na2SO3+H2O
(3)若滴加浓硫酸过快,则生成二氧化硫气体较快,可能导致二氧化硫气体来不及与B中的亚硫酸钠进一步反应生成Na2S2O5;故填:防止生成二氧化硫气体过快,来不及与B中的亚硫酸钠进一步反应生成Na2S2O5;
(4)该实验开始滴加浓硫酸时,应先除尽装置内的空气,是为了防止Na2S2O5被氧化成Na2SO4,这里反映了氧气的氧化性;故填:氧化性。

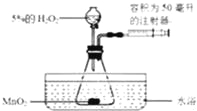
【题目】小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
实验1 | 实验2 | |
MnO2的质量/克 | 0.5 | 0.5 |
5%的H2O2的体积/毫升 | 40 | 待填 |
水浴温度/℃ | 20 | 80 |
(1)实验2中应加入5%H2O2 毫升。
(2)在两次实验中,可通过 来比较H2O2分解反应速率的大小。
(3)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因除锥形瓶内气体受热膨胀外,还有 。
(4)实验结束后若要将MnO2从混合物汇总分离出来,可采取的方法是 。