题目内容
【题目】请根据下列装置,回答问题:
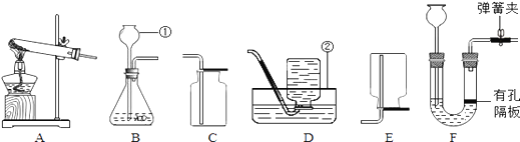
(1)写出标号①②的仪器名称:①________,②________。
(2)实验室用双氧水制取氧气可以选择的发生装置是________(填写装置序号),反应的文字表达式是________。
(3)若要收集较纯净的氧气,可选用的收集装置是________(填写装置序号)。若用C装置收集氧气,是因为根据氧气具有________的性质。要判断C中氧气是否集满,可________(填一操作),若看到________现象,则表明氧气已经收集满了。
(4)选用A装置加热高锰酸钾方法来制取氧气,采用D装置来收集氧气,同学发现水槽中的水变红了,操作上可能的原因是________。实验结束的时候应该先________,再________。
(5)一氧化氮是大气污染物,但少量一氧化氮在人体内具有扩张血管、增强记忆的功能。实验室收集一氧化氮只能用排水法收集。据此我们推测出一氧化氮具有的性质是________。(答出一点即可,但不可回答一氧化氮是一种气体)
(6)加热固体碳酸氢铵能产生二氧化碳,但实验室却不用加热分解碳酸氢铵的方法制取二氧化碳,理由是________ 。
(7)常温下,乙炔是一种无色气体,密度比空气略小,难溶于水。实验室常用碳化钙固体与饱和食盐水常温下反应来制取乙炔。现选择合适的装置来制取并收集较纯的乙炔,应该选择的发生装置是________(填序号,下同),收集装置是________。
【答案】长颈漏斗 水槽 B 过氧化氢![]() →水+氧气 D 氧气密度比空气大 将带火星的木条放在瓶口 木条复燃 A装置的试管口未放一团棉花 把导管从水中取出 熄灭酒精灯 难溶于水(或不与水反应或有毒等) 产生的气体中混有氨气等,制得的气体不纯 B或F D
→水+氧气 D 氧气密度比空气大 将带火星的木条放在瓶口 木条复燃 A装置的试管口未放一团棉花 把导管从水中取出 熄灭酒精灯 难溶于水(或不与水反应或有毒等) 产生的气体中混有氨气等,制得的气体不纯 B或F D
【解析】
(1)①②的仪器名称分别为长颈漏斗和水槽;
(2)实验室用双氧水制取氧气为固液在常温下反应,可以选择的发生装置是B;反应的文字表达式是过氧化氢![]() 水+氧气;
水+氧气;
(3)排水法收集的气体较排空气法纯净,所以若要收集较纯净的氧气,可选用的收集装置是D;C为向上排空气法收集,若用C装置收集氧气,是因为根据氧气的密度比空气大;判断是否集满的方法是将带火星的木条放在瓶口,若看到木条复燃则证明已满;
(4)高锰酸钾受热时会有颗粒进入导管,从而进入水槽,使水变红,所以为防止高锰酸钾颗粒进入导管,试管口要塞一团棉花,实验结束时要先将导管从水中移出,然后再熄灭酒精灯;
(5)实验室收集一氧化氮只能用排水法收集。据此我们推测出一氧化氮具有的性质是难溶于水、有毒等;
(6)加热固体碳酸氢铵能产生二氧化碳,但同时还会生成氨气和水蒸气,所以实验室不用加热分解碳酸氢铵的方法制取二氧化碳;
(7)实验室常用碳化钙固体与饱和食盐水常温下反应来制取乙炔,所以应选择固液常温型发生装置,即B或F;乙炔是一种无色气体,密度比空气略小,难溶于水,所以可用向下排空气法和排水法收集,若收集较纯净气体,则应选择排水法。

【题目】实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小科用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液),四组实验数据记录如下表,请分析计算:
实验组别 | 一 | 二 | 三 | 四 |
稀盐酸质量/g | 100.0 | 100.0 | 100.0 | 100.0 |
混合物质量/g | 3.0 | 6.0 | 9.0 | 12.0 |
所得溶液质量/g | 101.9 | 103.8 | 105.0 | a |
剩余固体质量/g | 0 | 0 | m | n |
(1)反应后,稀盐酸还有剩余的是第________组;
(2)求混合物中碳酸钙和氯化钙的质量之比________;
(3)求表中a的值为________;
(4)求表中m的值____。