题目内容
【题目】某同学设计了如图所示的探究Ca(OH)2溶解度随温度变化的实验。
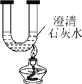
(1)向U形管中注入新配制的饱和澄清石灰水,用酒精灯对U形管的右侧加热,左管无明显变化,而右管中明显出现__________,这种现象称之为________(选填“结晶”或“蒸馏”),此时右管中溶液的溶质质量分数________(选填“增大”“减小”或“不变”);停止加热冷却至常温,能观察到右管中的____________消失,通过对比有效地证实了Ca(OH)2的溶解度随温度的________________的事实;
(2)上述U形管若敞口长期放置,澄清的石灰水表面会出现一层白膜,试写出有关反应的化学方程式:____________________________________。
【答案】 浑浊 结晶 减小 白色固体 升高而减小 Ca(OH)2+CO2===CaCO3↓+H2O
【解析】(1)氢氧化钙的溶解度随温度的升高而降低,加热时温度升高,氢氧化钙的溶解度减小析出氢氧化钙固体,溶液变浑浊,这种现象称为结晶,此时右管中溶液的溶质质量分数减小;停止加热冷却至常温,能观察到右管中的白色固体消失,通过对比有效地证实了Ca(OH)2的溶解度随温度的升高而减小的事实;(2)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2===CaCO3↓+H2O。

练习册系列答案
相关题目