题目内容
【题目】 Fe(OH)2和Fe(OH)3是两种常见的碱,白色的Fe(OH)2与空气中的氧气接触很快被氧化为红褐色Fe(OH)3,因此在实验室中制备Fe(OH)2,并使Fe(OH)2长时间保持白色沉淀状态,成为物质制备实验探究的热点。下面两种方法均可制得Fe(OH)2白色沉淀。
方法一:含FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)除去蒸馏水中溶解的O2常采用 _________ 的方法。
(2)生成Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是______ 。
方法二:在如下图所示的装置中,用NaOH溶液、碎铁皮、稀H2SO4等试剂制备。
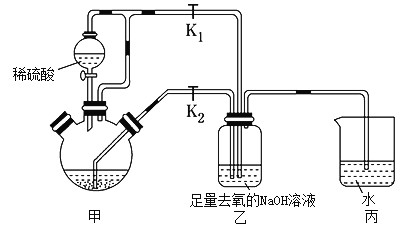
①检查装置气密性后,往三颈烧瓶甲中加入过量碎铁皮。
②关闭K2打开K1,旋开分液漏斗的旋塞并控制好滴速。
③待三颈烧瓶内的溶液由无色变成浅绿色时,把溶液转移到装置乙中,当出现大量白色沉淀时,关闭分液漏斗的旋塞。
(1)步骤②的目的__________。
(2)写出乙中有白色沉淀生成的反应的化学方程式_______。
(3)实现步骤③中溶液自动转移至装置乙中的实验操作为_________。
(4)装置丙中导管口水封的目的是_____________。
【答案】加热煮沸 避免将空气中的氧气引入反应体系 Fe与硫酸反应排出体系中的空气 ![]() 关闭K1 打开K2 防止空气进入乙装置
关闭K1 打开K2 防止空气进入乙装置
【解析】
方法一:
(1)加热煮沸可以除去蒸馏水中溶解的O2。故填:加热煮沸。
(2)硫酸亚铁与氢氧化钠反应生成Fe(OH)2,为防止氢氧化亚铁被氧化,用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,避免将空气中的氧气引入反应体系,可使Fe(OH)2长时间保持白色沉淀状态。故填:避免将空气中的氧气引入反应体系。
方法二:
(1)步骤②中稀硫酸滴下后会产生氢气和硫酸亚铁,产生的氢气会将装置中的空气排出,避免有氧气存在,使氢氧化亚铁变成氢氧化铁。故填:Fe与硫酸反应排出体系中的空气。
(2)浅绿色硫酸亚铁溶液进入乙中与氢氧化钠溶液反应产生氢氧化亚铁白色沉淀和硫酸钠,反应的化学方程式![]() 。故填:
。故填: ![]() 。
。
(3)实现步骤③中溶液自动转移至装置乙中的实验操作为关闭K1打开K2,这样产生的氢气不能排除,装置甲中的压强增大,将硫酸亚铁溶液压入到乙中。故填:关闭K1打开K2。
(4)装置丙中导管口水封的目的是防止空气进入乙装置,因为氧气进入会使生成的氢氧化亚铁变成氢氧化铁。故填:防止空气进入乙装置。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】(1)某兴趣小组在实验室相对封闭的装置内燃烧某种含碳、氢、氧元素的垃圾,对产生的废气成分(不考虑气态有机物)按如图所示的装置进行检验。
(实验研究)
拉动注射器,让废气依次通过装置。
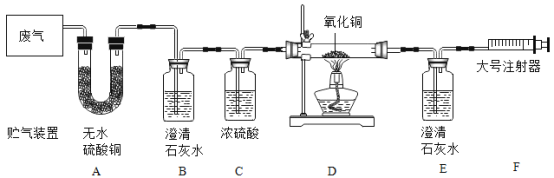
(实验分析)
①能证明废气中有水蒸气存在的现象是______;
②F处的大号注射器,可以引导气体流向,其另一个主要作用是______;
(反思评价)
③小金认为,仅根据E中澄清石灰水变浑浊,无法确定一氧化碳的存在,其理由是___;
④小金根据D中的粉末由黑色变为红色,得出废气中存在一氧化碳。小丽认为该结论不够严密,若废气中存在氢气也会出现该现象。要使上述结论更加严密,还应添加的一个实验装置________及位置是__。
(实验结果)经检验,废气中存在CO2、CO、H2O。
(2)已知金属钻(Co)的活动性与铁相似,请预测氯化钻(CoCl2)的化学性质,说明预测的依据,并设计实验验证。经查阅资料,钻的化合物相关性质如下:
物质 | CoO | Co(OH)2 | CoCl2 | CoSO4 | Co(NO3)2 | CoCO3 |
在水中溶的溶解性 | 难溶于水的灰绿色固体 | 难溶于水的粉红色固体 | 易溶于水形成粉红色溶液 | 易溶于水形成粉红色溶液 | 易溶于水形成粉红色溶液 | 难溶于水的粉红色固体 |
限选试剂:CoCl2溶液、(NH4)2CO3溶液、Na2SO4溶液、AgNO3溶液、NaOH溶液、稀硫酸、镁条、铜片。
预测 | 预测的依据 | 验证预测的实验操作与预期现象 |
①能够与含Ag+的可溶性盐反应 | CoCl2溶液中含Cl-,AgCl难溶于水。 | 取少量CoCl2溶液于试管中,加入少量AgNO3溶液,如果观察到有白色沉淀产生,则预测成立。 |
②能够与可溶性碱反应 | CoCl2溶液中含Co2+,______________ | 取少量CoCl2溶液于试管中,________,如果观察到___________,则预测成立。 |
③能够与___(填物质类别)反应 | ____________ | 取少量CoCl2溶液于试管中,_______,如果观察到___________,则预测成立。 |
【题目】小明在做实验时,不小心将镁条掉入到碳酸氢钠溶液中,发现产生大量的气泡和白色不溶物。他非常好奇,进行了如下探究。
实验探究1:镁条与碳酸氢钠溶液反应产生什么气体?
(提出猜想)
甲同学猜想:可能是二氧化碳
乙同学猜想:可能是氢气。
同学们作出猜想的依据是_____。
(设计实验)
将产生的气体收集起来,做如下实验:
实验步骤 | 实验现象 | 实验结论 |
①将收集的气体通入澄清石灰水中 | _____ | 甲同学猜想错误 |
②将收集的气体点燃 | 气体燃烧,产生_____火焰,有尖锐的爆鸣声 | 乙同学猜想正确 |
实验探究2:产生的白色不溶物是什么?
(查阅资料)
①Mg(OH)2难溶于水:MgCO3微溶于水:这两种物质受热都会分解成两种氧化物;
②白色无水CuSO4粉末遇水变蓝色。
(提出猜想)
猜想1:白色固体是Mg(OH)2
猜想2:白色固体是MgCO3
猜想3:_____。
(实验验证)
①取白色固体于试管中,滴加足量的稀盐酸,观察到有气泡产生,得出猜想1不正确,写出生该现象的反应化学方程式_____。
②小明通过进一步实验验证得出猜想3成立,写出实验操作及实验现象_____。