题目内容
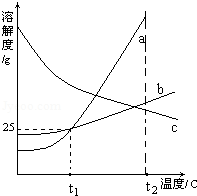
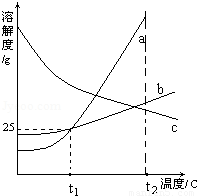
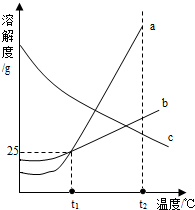 (2012?南充)如图为a、b、c三种物质(均不含结晶水)的溶解度曲线,据图回答下列问题.
(2012?南充)如图为a、b、c三种物质(均不含结晶水)的溶解度曲线,据图回答下列问题.①t1℃时,50g水中最多可溶解a物质
12.5
12.5
g.②t2℃时,a、b、c三种物质溶解度由大到小的顺序是
a>b>c
a>b>c
(填写物质序号)③将t1℃时a、b、c三种物质的饱和溶液升温至t2℃时,三种溶液的溶质质量分数大小是
a=b<c
a=b<c
(填写物质序号).分析:(1)根据t1℃时a物质的溶解度考虑;(2)根据某一温度时物质溶解度的比较方法考虑;(3)根据升温后溶质和溶剂的变化考虑.
解答:解:(1)t1℃时a物质的溶解度为25g,即100g水中最多溶25g,则50g水中最多溶12.5g;
(2)从t2℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t2℃时它们的溶解度大小顺序:a>b>c;
(3)饱和溶液的质量分数:
×100%,所以饱和溶液的质量分数与溶解度有关,溶解度大质量分数就大,t1℃时a、b、c三种物质的溶解度是c>a═b,所以t1℃时a、b、c三种物质饱和溶液的质量分数也是c>a═b,升温后,a和b变为不饱和,溶质质量分数没变,所以还是a═b,c物质升温后溶解度变小,析出晶体,仍然饱和,但t2℃时c的溶解度也比t1℃时a、b物质的溶解度大,所以升温后三种溶液的溶质质量分数大小是a=b<c.
故答案为:(1)12.5;(2)a>b>c;(3)a=b<c.
(2)从t2℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t2℃时它们的溶解度大小顺序:a>b>c;
(3)饱和溶液的质量分数:
| 溶解度 |
| 100g+g溶解度 |
故答案为:(1)12.5;(2)a>b>c;(3)a=b<c.
点评:本题容易出错的地方是对升温后溶质质量分数的判断,要知道饱和溶液的质量分数与溶解度有关,溶解度大质量分数就大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(2012?南充)在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
(1)小明同学选用如图所示的装置制取氧气.
制取过程中所发生的化学反应方程式为: .
实验前小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现.该实验操作的目的是 .
(2)小红同学通过互联网得知:CuSO4溶液、动物某些脏器中含有的物质等能催化过氧化氢的分解.
动物脏器中含有过氧化氢酶,能催化过氧化氢分解,过氧化氢酶是 (选填序号填空:①糖类、②蛋白质、③脂肪、④维生素)
实验证明,在过氧化氢溶液中滴加CuSO4溶液能显著加快过氧化氢的分解.CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42﹣),为了进一步探究CuSO4溶液中哪种粒子能起催化作用.小红同学作了以下分析和设计.
①小红同学认为最不可能的是H2O,他的理由是 .
②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验,完成了这次探究活动.
| 实验步骤 | 实验现象 | 结论 |
| a.取一支试管加入5mL5%过氧化氢溶液,然后加入2﹣3滴稀硫酸 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是 . |
| b.另取一支试管加入5mL5%过氧化氢溶液,然后加入2﹣3滴 溶液 | 溶液中有大量气泡放出 |
 (2012?南充)在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
(2012?南充)在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.