题目内容
某实验小组设计了实验室制取二氧化碳气体所用药品的三个方案:方案一,粉末状碳酸钙与稀盐酸;
方案二,块状石灰石与稀盐酸;
方案三,块状石灰石与浓盐酸.
三个方案中,最好的方案是 ,其理由是 .
解答:解:方案一:粉末状碳酸钙易于稀盐酸充分接触,立刻生成二氧化碳,不利于收集,故此方案不合适;
方案二:块状石灰石与稀盐酸只在石灰石表面接触,面积较小,生成二氧化碳速度较慢,便于收集,故此方案合适;
方案三:浓盐酸极易挥发,生成的气体中易混入盐酸蒸汽,故此方案不适合.
故答案为:方案二、其一,反应速度适度,便于气体收集;其二,生成的二氧化碳气体较纯.
点评:本题考查的是实验室制取二氧化碳的方法,在制取气体时首先要考虑收集方便,其次要考虑气体的纯度.

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案氢氧化钾是我国古代纺织业常用的洗涤剂,先秦科技著作《周礼· 考工记》中记载:“练帛,以栏为灰,渥淳其帛,实诸泽器,淫之以蜃,清其灰而盝之……”。这是介绍了古代精练丝绸的步骤:I.丝绸放在光滑的容器里要用草木灰水(主要成分是碳酸钾)浸润透;II.将一定量蚌壳(蚌壳主要成分为碳酸钙)灼烧成的蚌壳灰加入上述容器中一起浸泡。这样就能产生碱性较强的氢氧化钾……
某实验小组设计如下实验以验证数千年前氢氧化钾制取方法。
| 序号 | 实验步骤 | 现象 |
| ① | 将少量蚌壳灼烧成的灰,放入装有较多水的大烧杯中; | 水的温度升高。 |
| ② | 向烧杯中加入较多草木灰(碳酸钾过量); |
|
| ③ | 实验操作甲; | 分别得到澄清溶液和固体; |
| ④ | 取少量溶液加入试管中,滴加足量试剂A; | 有白色沉淀产生; |
| ⑤ | 再向试管中滴加无色酚酞; | 溶液显红色 |
实验分析:
(1)实验步骤②中发生反应的方程式为 。
(2)第③步实验操作甲的名称为 ;
(3)第④步实验所用试剂A为 ;必须有第④步实验的原因是
。
(4)下列试剂可以代替第⑤步实验中的无色酚酞的有 。
A.氧化铁 B.二氧化碳 C.氢氧化钠溶液 D.硫酸铜溶液
氢氧化钾是我国古代纺织业常用的洗涤剂,先秦科技著作《周礼· 考工记》中记载:“练帛,以栏为灰,渥淳其帛,实诸泽器,淫之以蜃,清其灰而盝之……”。这是介绍了古代精练丝绸的步骤:I.丝绸放在光滑的容器里要用草木灰水(主要成分是碳酸钾)浸润透;II.将一定量蚌壳(蚌壳主要成分为碳酸钙)灼烧成的蚌壳灰加入上述容器中一起浸泡。这样就能产生碱性较强的氢氧化钾……
某实验小组设计如下实验以验证数千年前氢氧化钾制取方法。
|
序号 |
实验步骤 |
现象 |
|
① |
将少量蚌壳灼烧成的灰,放入装有较多水的大烧杯中; |
水的温度升高。 |
|
② |
向烧杯中加入较多草木灰(碳酸钾过量); |
|
|
③ |
实验操作甲; |
分别得到澄清溶液和固体; |
|
④ |
取少量溶液加入试管中,滴加足量试剂A; |
有白色沉淀产生; |
|
⑤ |
再向试管中滴加无色酚酞; |
溶液显红色 |
实验分析:
(1)实验步骤②中发生反应的方程式为 。
(2)第③步实验操作甲的名称为 ;
(3)第④步实验所用试剂A为 ;必须有第④步实验的原因是
。
(4)下列试剂可以代替第⑤步实验中的无色酚酞的有 。
A.氧化铁 B.二氧化碳 C.氢氧化钠溶液 D.硫酸铜溶液
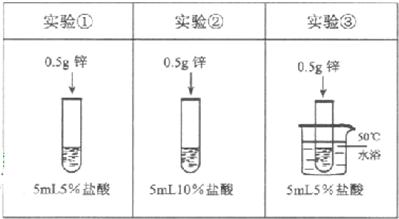
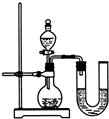 物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
物质之间发生化学反应时,常伴随有明显的现象,但有些化学反应却观察不到明显的现象.某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
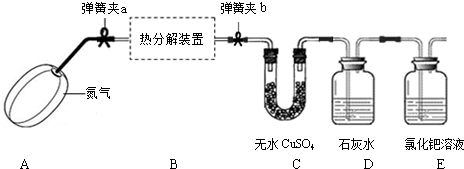
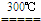 FeO+CO2↑+CO↑+2H2O
FeO+CO2↑+CO↑+2H2O