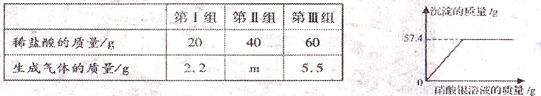
题目内容
取47.4g高锰酸钾,加热一段时间后停止,共收集到3.2g氧气.计算:
(1)参加反应的高锰酸钾的质量.
(2)剩余固体中氧元素的质量分数(计算结果保留到0.1%).
(1)31.6g (2)36.2%
解析试题分析:(1)设参加反应的高锰酸钾的质量为x
设参加反应的KMnO4质量为x
2KMnO4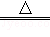 K2MnO4 +MnO2 +O2↑
K2MnO4 +MnO2 +O2↑
316 32
x 3.2g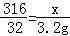 解得:x=31.6g
解得:x=31.6g
(2)剩余固体中氧元素的质量分数 =36.2%.
=36.2%.
答:(1)参加反应的高锰酸钾的质量是31.6g;(2)剩余固体中氧元素的质量分数是36.2%.
考点:根据化学反应方程式的计算;化合物中某元素的质量计算
点评:此题主要考查有关化学方程式的计算,通过认真分析题干,利用质量守恒定律可直接得到剩余固体中氧元素的质量,再除以混合物的质量可轻松解决.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
下表列出一氧化氮的部分性质(已知:空气在20℃时的密度是1.293 g / L)
| 物理性质 | 化学性质 | |||
| 熔点 | 沸点 | 密度(20℃) | 溶解性 | |
| -163.64℃ | -151.76℃ | 1.249 g / L | 不易溶于水 | 2NO+O2=2NO2 |
A.向上排气法 B.排水法 C.向下排气法 D.向下排气法或排水法