题目内容
 微量元素是人体必须的元素.铁是人体必须的微量元素之一,摄入量不足会因缺铁而引起疾病.如图是某补铁剂的部分标
微量元素是人体必须的元素.铁是人体必须的微量元素之一,摄入量不足会因缺铁而引起疾病.如图是某补铁剂的部分标签,根据所学知识回答问题:
(1)实验室要用废铁屑与稀硫酸反应制取硫酸亚铁.反应前要除去废铁屑表面的油污,洗涤油污所用的溶液是
A.碳酸钠溶液 B.稀盐酸
C.氢氧化钠溶液 D.石灰水
(2)制取硫酸亚铁的反应中,反应前后化合价发生变化的元素是
(3)根据标签中的信息计算,服用一片该药相当于补铁
考点:标签上标示的物质成分及其含量,常用盐的用途,有关元素化合价的计算,化合物中某元素的质量计算
专题:标签图示型
分析:(1)反应前要除去废铁屑表面的油污,据此结合碳酸钠、稀盐酸、氢氧化钠、石灰水的用途进行分析解答.
(2)铁屑与稀硫酸反应生成硫酸亚铁和氢气,根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(2)铁屑与稀硫酸反应生成硫酸亚铁和氢气,根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:(1)碳酸钠溶液和氢氧化钠溶液能与油脂反应,可以洗涤油污,可除去废铁屑表面的油污.
(2)铁屑与稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式是Fe+H2SO4=FeSO4+H2↑;反应前氢元素的化合价为+1价,反应后化合价为0价;反应前,铁元素的化合价为0价,反应后变为+2价,故发生变化的元素是氢元素和铁元素,元素符号为H和Fe.
(3)由题意,一片含主要成分硫酸亚铁0.16g,则服用一片该药相当于补铁的质量=0.16g×
×≈0.06g.
故答案为:(1)AC;(2)H和Fe;(3)0.06.
(2)铁屑与稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式是Fe+H2SO4=FeSO4+H2↑;反应前氢元素的化合价为+1价,反应后化合价为0价;反应前,铁元素的化合价为0价,反应后变为+2价,故发生变化的元素是氢元素和铁元素,元素符号为H和Fe.
(3)由题意,一片含主要成分硫酸亚铁0.16g,则服用一片该药相当于补铁的质量=0.16g×
| 56 |
| 56+32+16×4 |
故答案为:(1)AC;(2)H和Fe;(3)0.06.
点评:本题难度不大,考查同学们结合标签新信息、灵活运用常见酸碱盐的用途与化学式的有关计算等进行分析问题、解决问题的能力.

练习册系列答案
相关题目

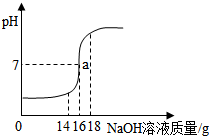 将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答:
将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答:
 人体胃酸过多会引起胃病.如图所示为某抗酸药包装标签上的部分文字,请回答下列问题.
人体胃酸过多会引起胃病.如图所示为某抗酸药包装标签上的部分文字,请回答下列问题.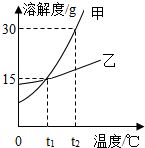 如图为甲、乙两种固体物质的溶解度曲线,请根据图示回答下列问题:
如图为甲、乙两种固体物质的溶解度曲线,请根据图示回答下列问题: