题目内容
【题目】下图是实验室制取气体常用的装置,试回答:
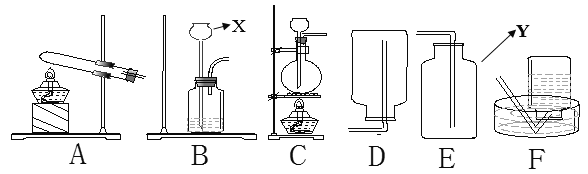
(1)写出下列仪器的名称: X_________________ Y_____________
(2)若用过氧化氢制取较纯净的氧气,应该选用_________和_________装置;若用高锰酸钾制取氧气且用排空气法收集,则应当选用_________和_________装置,反应的化学方程式:____________________________________________________。
(3)用排水气法收集氧气时,当观察到______________________________时,说明集气瓶中已充满氧气。
(4)当用排空气法收集氧气时,这是依据氧气_________________________________ 的性质。怎样检验集气瓶中是否已充满氧气?____________________________________________________。
【答案】 长颈漏斗 集气瓶 B F A E 2KMnO4![]() K2MnO4+MnO2+O2↑ 水面产生气泡 氧气的密度比空气大 用带火星的木条放在集气瓶口,若木条复燃则已满
K2MnO4+MnO2+O2↑ 水面产生气泡 氧气的密度比空气大 用带火星的木条放在集气瓶口,若木条复燃则已满
【解析】(1)据图可知仪器的名称:X是长颈漏斗;Y是集气瓶;(2)若用过氧化氢制取氧气不需要加热,发生装置选用B,密度比空气大,可用向上排空气法收集,但排水法收集的氧气较为纯净,收集装置选F;用高锰酸钾制取氧气属于加热固体制取气体,发生装置选A;密度比空气大,可用向上排空气法收集,收集装置选E;反应的化学方程式:2KMnO4△ K2MnO4+MnO2+O2↑;(3)用排水气法收集氧气时,当观察到水面产生气泡时,说明集气瓶中已充满氧气;(4)氧气的密度比空气大,可用向上排空气法收集;用带火星的木条放在集气瓶口,若木条复燃则已满。
【题型】实验题
【结束】
30
【题目】已知在高温条件下一氧化碳可以和氧化铁(Fe2O3)发生反应生成铁和一种能使澄清石灰变浑浊的气体。现有56g一氧化碳和足量的氧化铁发生反应,根据题意回答下列问题:
(1)计算氧化铁的相对分子质量_______________。
(2)根据已知条件写出该反应的化学方程式__________________________________。
(3)计算理论上56g一氧化碳可以和__________g氧化铁发生反应。
【答案】 Fe2O3 =56 *2+16*3=160 Fe2O3+3CO![]() 2Fe+3CO2 140g
2Fe+3CO2 140g
【解析】解:(1)氧化铁的相对分子质量为: ![]() ;(2)在高温条件下一氧化碳可以和氧化铁(Fe2O3)发生反应生成铁和一种能使澄清石灰变浑浊的气体,该反应的化学方程式为:Fe2O3+3CO
;(2)在高温条件下一氧化碳可以和氧化铁(Fe2O3)发生反应生成铁和一种能使澄清石灰变浑浊的气体,该反应的化学方程式为:Fe2O3+3CO![]() 2Fe+3CO2;(3)设需要氧化铁的质量为x,
2Fe+3CO2;(3)设需要氧化铁的质量为x,
Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
160 84
x 56g
![]()
x=140g。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案