��Ŀ����
����Ŀ�������Ǽ���ʵ������ȡ����ķ���װ�����ռ�װ�á�
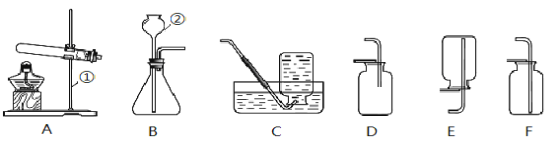
��1��д���б�ŵ��������ƣ��� ��
��2�����ø��������ȡ����ʱ����ѡ�õķ���װ���� __������ĸ��ţ���ͬ�����ռ�װ����C�� ����Ӧ�ķ��ű���ʽΪ
��3������Cװ���ռ���������ȷ�IJ���˳��Ϊ �����ţ���
a�����������뼯��ƿ�ڣ����������ƿ��
b����װ��ˮ�ļ���ƿ������ˮ����
c���������ռ���ʱ����ë����Ƭ��סƿ�ڣ�������ƿ�Ƴ�ˮ��������������
��4�����ù���������Һ�Ͷ���������ȡ������Ϊ�˿��Ʒ�Ӧ���ʣ����ƽ�ȵ����������� ����һ���������ƣ�����Bװ���е������ڡ�
��5��������NH3����һ����ɫ�д̼�����ζ�����壬�ܶȱȿ���С�Ҽ�������ˮ��ʵ�����ü����Ȼ�狀���ʯ�ҵĹ���������ȡ��������ѡ����ͼ�е�G��H����ռ�����������Ӧ�� ���a����b������ͨ�룬��һ�˽�Hװ���е�c��װ����©���������� ��
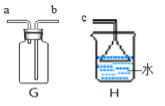
��6��ʵ������ȡ������̼��
��һ��ѡ��ĵ�ҩƷ�� ��ϡ���ᣬ��Ӧ�ķ��ű���ʽΪ ��
��Ϊ�˼��������̼����ѡ��Gװ�ã�ƿ���ȷ������� �����Լ����ƣ���Ȼ������� ����a��b����ͨ�룬��Ӧ�ķ��ű���ʽΪ ��
��������ͼ���ұ���ѡ����ʵ�װ����ȡ������̼���ܴﵽ���濪���ã������ͣ��Ŀ�ĵ��� �����ţ�

��7����ͼ�ǡ���˿��������ȼ�ա�ʵ��ĸĽ�װ�ã�ʵ��ʱ����ҹ©��������ͨ���������Լ10�룬��ȼ��˿�¶˻��ˣ���������ƿ�ڣ����������ܿ����Ϸ����۲쵽�������ǣ���˿����ȼ�գ� ��
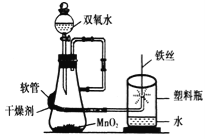
�Ľ���װ�þ��е��ŵ��� ������ţ���
������������ǰ�Ʊ����ռ�������������
������ƿ���漯��ƿ����ֹ����ƿը�ѣ�����ȫ
��װ�ü���������ȡ�������������֤��һ�壬ʵ����Ż�
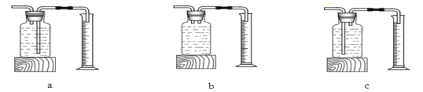
��8��С����ʦ����ѧ��������������ʵ��ʱ�����֡�һͬѧ��������װ�������ļ���ƿ��Ѹ�ٷ����ƿ��ʣ�����������ʹ�����ǵ�ľ����ȼ�����Դˣ�С����ʦ�ø�ͬѧ������ƿװ���ƿˮ��������ˮ���ռ�1/2����ƿ������������ƿ�е�����Ҳ��ʹ������ľ����ȼ��
�������з����ռ���1/2����ƿ����������������������� ������ĸ����
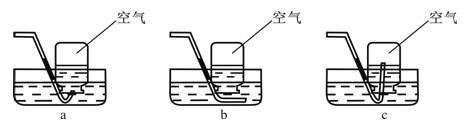
������ˮ���ռ�����ʱ������ƿ���������ռ���ʱ��������
�ۿ������������������ԼΪ21%����ʵ���У�����ƿ�ڵ�����Լռ������� ��
���𰸡���1������̨������©��
��2��A��F ��2KMnO4![]() K2MnO4+MnO2+O2��
K2MnO4+MnO2+O2��
��3��bac
��4����Һ©��
��5��a����ֹ������������
��6���ٴ���ʯ��CaCO3 + 2HCl==CaCl2 + CO2�� + H2O����ʯ��ˮ��b��Ca��OH��2+CO2===H2O+CaCO3���ۼ���
��7����������
��8����a�������ƿ����ð����60.5%
��������
����������ø��������ȡ����ʱ����ѡ�õķ���װ����A����Ϊ��Ҫ���ȣ��ռ�װ����C��F����Ϊ�������ܶȴ��ڿ������Ҳ�������ˮ�У���Ӧ�ķ��ű���ʽΪ2KMnO4![]() K2MnO4+MnO2+O2��������Cװ���ռ���������ȷ�IJ���˳��Ϊ����װ��ˮ�ļ���ƿ������ˮ���С����������뼯��ƿ�ڣ����������ƿ�С��������ռ���ʱ����ë����Ƭ��סƿ�ڣ�������ƿ�Ƴ�ˮ�������������棻���ù���������Һ�Ͷ���������ȡ������Ϊ�˿��Ʒ�Ӧ���ʣ����ƽ�ȵ����������÷�Һ©������Bװ���е������ڡ���ѡ����ͼ�е�G��H����ռ�����������Ӧ��a��ͨ�룬��Ϊ�������ܶ�С�ڿ�������һ�˽�Hװ���е�c��װ����©���������Ƿ�ֹ������������һ��ѡ��ĵ�ҩƷ�Ǵ���ʯ��ϡ���ᣬ��Ӧ�ķ��ű���ʽΪCaCO3 + 2HCl==CaCl2 + CO2�� + H2O��Ϊ�˼��������̼����ѡ��Gװ�ã�ƿ���ȷ�������ʯ��ˮ��Ȼ�������b��ͨ�룬��Ӧ�ķ��ű���ʽΪCa��OH��2+CO2===H2O+CaCO3����ʵ��ʱ����ҹ©��������ͨ���������Լ10�룬��ȼ��˿�¶˻��ˣ���������ƿ�ڣ����������ܿ����Ϸ����۲쵽�������ǣ���˿����ȼ�գ��������䣮�Ľ���װ�þ��е��ŵ��ǣ�����������ǰ�Ʊ����ռ������������㣻�����з����ռ���1/2����ƿ�����������������������a������ˮ���ռ�����ʱ������ƿ���������ռ���ʱ�������������ƿ����ð�����������������������ԼΪ21%����ʵ���У�����ƿ�ڵ�����Լռ�������=50%+50%*21%=60.5%��
K2MnO4+MnO2+O2��������Cװ���ռ���������ȷ�IJ���˳��Ϊ����װ��ˮ�ļ���ƿ������ˮ���С����������뼯��ƿ�ڣ����������ƿ�С��������ռ���ʱ����ë����Ƭ��סƿ�ڣ�������ƿ�Ƴ�ˮ�������������棻���ù���������Һ�Ͷ���������ȡ������Ϊ�˿��Ʒ�Ӧ���ʣ����ƽ�ȵ����������÷�Һ©������Bװ���е������ڡ���ѡ����ͼ�е�G��H����ռ�����������Ӧ��a��ͨ�룬��Ϊ�������ܶ�С�ڿ�������һ�˽�Hװ���е�c��װ����©���������Ƿ�ֹ������������һ��ѡ��ĵ�ҩƷ�Ǵ���ʯ��ϡ���ᣬ��Ӧ�ķ��ű���ʽΪCaCO3 + 2HCl==CaCl2 + CO2�� + H2O��Ϊ�˼��������̼����ѡ��Gװ�ã�ƿ���ȷ�������ʯ��ˮ��Ȼ�������b��ͨ�룬��Ӧ�ķ��ű���ʽΪCa��OH��2+CO2===H2O+CaCO3����ʵ��ʱ����ҹ©��������ͨ���������Լ10�룬��ȼ��˿�¶˻��ˣ���������ƿ�ڣ����������ܿ����Ϸ����۲쵽�������ǣ���˿����ȼ�գ��������䣮�Ľ���װ�þ��е��ŵ��ǣ�����������ǰ�Ʊ����ռ������������㣻�����з����ռ���1/2����ƿ�����������������������a������ˮ���ռ�����ʱ������ƿ���������ռ���ʱ�������������ƿ����ð�����������������������ԼΪ21%����ʵ���У�����ƿ�ڵ�����Լռ�������=50%+50%*21%=60.5%��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��ˮ�DZ������Ȼ��Դ���ڹ�ũҵ�������ճ����������ż���㷺�����á�
��һ��ˮ��Դ����״��
��1�� �ҹ���ˮ����ȱˮ��֮�У��˾���ˮ��Դ��Ϊ�����˾�����1��4����������Щ��ׯ���ȡ�õ���ˮ���������ˮ��Ӳˮ������ˮ������ȡˮ���������� ����������ĭ�٣��н϶ม��������˵����Ӳˮ��ʹ��Ӳˮ�����������������鷳�������г��� �ķ���������ˮ��Ӳ�ȡ�
������ˮ�ľ���
��2��С���ռ���һƿ���ǵĺ�ˮ����Ҫģ������ˮ���ľ�ˮ���̣������Ƴ�����ˮ����ʵ���������ͼ��ʾ����ͼ��A������һ�������������������� �������ٵ����� ����������Ҫ�dz�ȥˮ�е�һЩ��ζ��ɫ�أ�Ӧѡ�õ�������

��3����ˮ������Ҫ��Ϊ���ṩ����ˮ��ũҵ��ˮ��Ŀǰ����Ĥ�����г��е��������߷��Ӱ�Ĥֻ����ˮ�����������ʲ���������ˮ������������ �仯�������������ѧ������
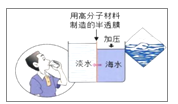
������ˮ��Դ������
��4��ˮ�����������г������ܽ������γ���Һ��ʵ�����ܽ�����ʱ���õ��IJ����������ձ���
��5��ˮһ����Ҫ��Ӫ�����ʣ�����Ϊ������Ӫ���ء�֮�ס� ������Һʱ����������ˮ��0��9%���Ȼ�����Һ����ҽ��������ˮ�� ��ѡ����������������
��6���ֽ�ˮ���Եõ�������������һ�ֿ�ȼ�����塣��������ࡢ��Ч����ȫ�������桢�����������ŵ㣬����Ϊ�����������ɫ��Դ����
��ͼ�ǵ��ˮ�ļ�װ�ã�����ͼ�������жϣ����Թ��ڵ���������� �����飻ʵ��֤��ˮ���� ��ɵģ�
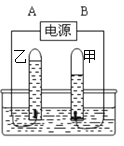
���ˮҪ���Ĵ����ĵ��ܣ���ѧ����������������������ˮ������������TiO2�������������տɷֽ�ˮ�õ��������÷�Ӧ�û�ѧʽ��ʾΪ ��
��7���±�����ȤС��ͬѧһ�ε��ˮʵ���õ�ʵ�����ݣ�
���ʱ�� | 1 | 2 | 3 | 4 | 5 | 6 | �� |
���������������/mL | 6 | 12 | 20 | 29 | 39 | 49 | �� |
���������������/mL | 2 | 4 | 7 | 11 | 16 | 21 | �� |
�������е������㷢�ֵ������� ��������һ�����ԭ������� ��
��8������֪ͨ��״����������ܶȣ�H2 : 0��089g/L O2: 1��429 g/L�����Ը��ݵ��ˮ���������������������������ֵ�������������������������������Ϊ �U �����ȡ������
����Ŀ������Ϊʵ���ҳ��õ�ʵ��װ�ã��ش�����
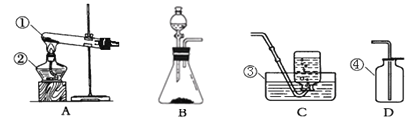
��1����д���б�����������ƣ��� ���� ��
��2��ʵ�����ø������������Ӧѡ�õķ���װ���� �����������װ��ҩƷǰӦ�� ������Cװ���ռ�O2���������ռ����ʱ��Ӧ��__ �����������װ���ռ������������������ܵ�ԭ���� �����������������Ӧ�����ֱ���ʽ�� ��
��3��ʵ������CO2��Ӧ���ֱ���ʽΪ �����⣬Ҳ���ü���̼��������NaHCO3������������Ϊ̼���ơ�������̼��ˮ������ȡCO2���÷�ӦӦѡ�õķ���װ��Ϊ ���ռ�����װ�� ��ʵ���Ҳ����ü���̼����粒�������ȡCO2��ԭ���� ��
��4��������ͼEװ���ռ�����Ӧ�� ���������a����b�����������������ķ����� ������E��װ��ˮ����ˮ�����ռ�����Ӧ�� ��������
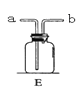
��5����B��ȡ������A��ȡ�������ŵ��� ����������
A��������ֻ������ B����Ӧ������Ƚ���
C�����ڿ��Ʒ�Ӧ���� D��������Ի���û����Ⱦ
��6��ij��ѧ��ȤС��ѧϰ����������MnO2�����ֽ���������ʵ���������ʵ�飺a�� ѡ��װ�ò���������ԡ�b����ȡ0��1�˵Ķ���������MnO2����ĩ���������С�c����ȡ50����������������Լ5%�Ĺ���������Һ���������У���¼һ��ʱ�����ռ���������������ı�������̵��������ظ�����ʵ�飬��¼�������¡����ܽˮ�е��������Բ�����
ʱ��/�� | �������������/���� | |||
0��1��MnO2 | 0��2��MnO2 | 0��3��MnO2 | 0��4��MnO2 | |
40 | 49 | 61 | 75 | 86 |
80 | 77 | 87 | 90 | 92 |
120 | 89 | 92 | 92 | 92 |
160 | 92 | 92 | 92 | 92 |
��д������������Һ��������̻������ȡ������Ӧ�����ֻ���ű���ʽ ��
�ڸ�ѧϰС��������������װ���е� ���A����B����������װ���е� �����������Ӳ���O2�������
��ʵ����ۣ�����ͬ�����£� ��˫��ˮ�ֽ��Խ�졣
��ʵ�鷴˼��������ʵ���õ������������ƫ��Ŀ���ԭ���� ��


