题目内容
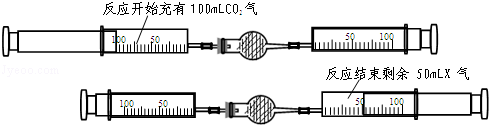
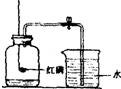
在红磷燃烧测定空气中氧气含量的实验中,若红磷燃烧时,没有夹紧止水夹,后果是 。如果操作正确,该实验能得出的结论是 。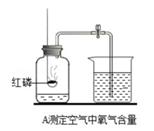
测量结果偏大 氧气占空气总体积的五分之一
解析试题分析:在测定空气中氧气含量的实验中,如果红磷燃烧时,没有夹紧止水夹,密封装置内的一部分气体在燃烧过程中会跑到空气中,实验完毕冷却到室温后,使得密封装置内的气体压强比正常情况下减少的更多,所以进入的水的体积会更大,正常情况下进入水的体积应为集气瓶容积的五分之一。
考点:空气中氧气含量的测定。

练习册系列答案
相关题目
如图是水的电解实验。
(1)写出该化学反应的化学方程式 ,该反应属于 。
(2)该实验的主要目的是 。
| A.观察水分解的现象 | B.研究水分解产物的性质 |
| C.探究水分解的条件 | D.验证水由氧元素和氢元素组成 |
(4)检验b管中产物的方法是用带火星的木条接近玻璃管尖嘴部分,慢慢打开活塞,看到的现象 。
水是宝贵的自然资源,水资源不足,将严重影响人类的生存。
(1)无论是自来水还是纯净水,保持水的化学性质的最小粒子是__________。
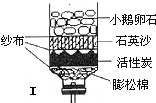
(2)自制简易净水器常加入______用于除去水中的异味和色素,属于_______(“物理变化”或“化学变化”)。
(3)小磊对水进行了下列实验,其中能确定水由氢元素和氧元素组成的是______(填序号)。
| A.蒸发 | B.电解 | C.沉淀 | D.吸附 |
(5)为了保护水资源,说说你在生活中节约用水的具体做法:_______________。
化学就在我们身边,它能改善我们的生活。请从“
| A.氧气 | B.氮气 | C.水 | D.二氧化硫E.明矾”中选择适当的物质填空(填字母): |
(2)充填于食品包装袋内以防食品变质的是 ;
(3)排放到空气易造成空气污染的是 。