题目内容
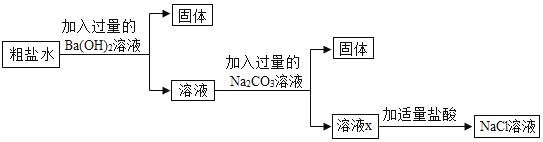
【题目】某工厂的废液中,含有较多的CuSO4和FeSO4两种物质。工厂常用下列流程将废液充分利用:
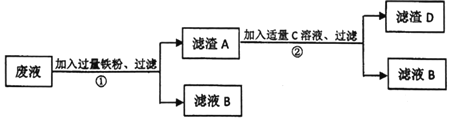
(1)写出步骤①中发生的化学反应方程式______,为什么要加入过量的铁粉______。
(2)写出步骤②中发生的化学反应类型是______。
(3)写出滤渣D的化学式______。
(4)将步骤①和②中产生的滤液B混合进行结晶,此操作过程需要用到的玻璃仪器名称是______![]() 任写一种即可
任写一种即可![]()
【答案】Fe+CuSO4=FeSO4+Cu 使硫酸铜完全反应 置换反应 Cu 玻璃棒
【解析】
(1)步骤①中铁和硫酸铜反应生成硫酸亚铁和铜,发生的化学反应方程式为:Fe+CuSO4=FeSO4+Cu,加入过量的铁粉是为了使硫酸铜完全反应;
(2)滤渣A中存在铜和铁,步骤②中,铜不能与硫酸反应,铁和稀硫酸反应生成硫酸亚铁和氢气,该反应是由一种单质与一种化合物反应生成另一种单质与另一种化合物的反应,属于置换反应;
(3)根据流程图可知,滤渣D是铜,化学式是Cu;
(4)将步骤①和②中产生的滤液B混合进行结晶,此操作过程是蒸发,需要用到的玻璃仪器有玻璃棒等;

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
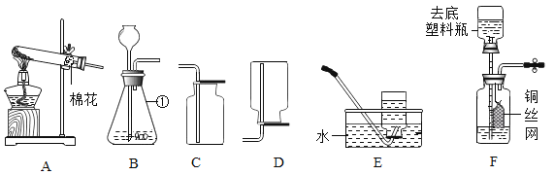
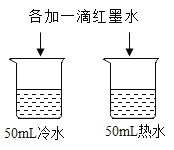
【题目】对比实验是实验探究的重要方法,下列对比实验设计能实现相应实验目的的是
选项 | 实验目的 | 实验设计 | 选项 | 实验目的 | 实验设计 |
A | 探究温度对分子运动快慢的影响 |
| B | 探究水对铁钉锈蚀的影响 |
|
C | 探究空气是燃烧的必要条件 |
| D | 探究CO2与水反生反应 |
|
A. A B. B C. C D. D