题目内容
 碘元素是人体必需的微量元素之一.
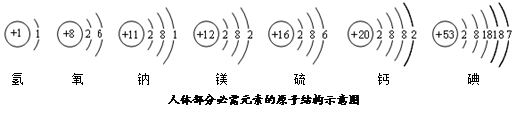
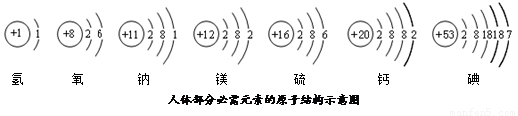
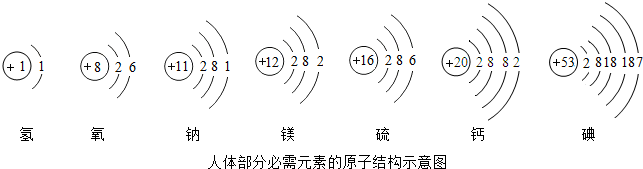
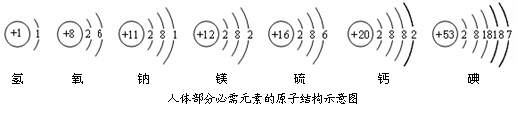
碘元素是人体必需的微量元素之一.(1)如图是元素周其表中碘元素的部分信息.碘原子的核电核荷数
53
53
;碘元素属于非金属
非金属
(填“金属”或“非金属”).(2)已知某碘盐的成分是氯化钠和碘酸钾(KIO3).
①氯化钠的化学式为
NaCl
NaCl
;KIO3中I的化合价为+5
+5
;②已知每包碘盐中含碘酸钾(KIO3)25.3mg,则每包碘盐中含有碘
15
15
mg.(取整数)(3)用化学符号填空:①2个氮原子
2N
2N
;②2个硫酸根离子2SO42-
2SO42-
.分析:(1)根据元素周期表中的一个小格所提供的信息,其中原子序数=核外电子数=质子数,进行解答;
根据化学元素汉字名称的偏旁可辨别元素的种类,固态非金属元素名称有“石”字旁;
(2)①氯化钠含有的阴离子是氯离子,阳离子是钠离子进行解答;根据“在化合物中,正负化合价的代数和为零”的原则,解答KIO3中I的化合价;
②根据某元素的质量=该物质的质量×该元素的质量分数进行解答;
(3)根据在元素符号前面加数值表示原子个数、在离子符号前面加数值表示离子个数进行解答.
根据化学元素汉字名称的偏旁可辨别元素的种类,固态非金属元素名称有“石”字旁;
(2)①氯化钠含有的阴离子是氯离子,阳离子是钠离子进行解答;根据“在化合物中,正负化合价的代数和为零”的原则,解答KIO3中I的化合价;
②根据某元素的质量=该物质的质量×该元素的质量分数进行解答;
(3)根据在元素符号前面加数值表示原子个数、在离子符号前面加数值表示离子个数进行解答.
解答:解:(1)根据元素周期表中的一个小格所提供的信息,可知碘原子的核电荷数是 53,根据化学元素汉字名称的偏旁可辨别元素的种类,固态非金属元素名称有“石”字旁;因此碘元素属于非金属元素;
(2)①氯化钠的化学式为:NaCl;
根据“在化合物中,正负化合价的代数和为零”的原则,可得KIO3中I的化合价为:(+1)+x+(-2)×3=0;x=+5;
②每包碘盐中最多含KIO3的质量为25.3mg,则碘元素的质量为:25.3mg×
×100%=15mg.
(3)①2个氮原子:2N;②2个硫酸根离子:2SO42-.
故答案为:
(1)53;非金属;
(2)①NaCl;+5;②15;(3)①2N;②2SO42-.
(2)①氯化钠的化学式为:NaCl;
根据“在化合物中,正负化合价的代数和为零”的原则,可得KIO3中I的化合价为:(+1)+x+(-2)×3=0;x=+5;
②每包碘盐中最多含KIO3的质量为25.3mg,则碘元素的质量为:25.3mg×
| 126.9 |
| 39+126.9+16×3 |
(3)①2个氮原子:2N;②2个硫酸根离子:2SO42-.
故答案为:
(1)53;非金属;
(2)①NaCl;+5;②15;(3)①2N;②2SO42-.
点评:本题考查学生对化合价计算及根据物质中某元素的质量及质量分数计算方法的掌握与在解题中应用的能力.

练习册系列答案
相关题目

 依图填空:
依图填空: ▲ ;
▲ ;