题目内容
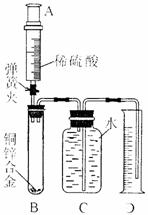
某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)
 探究过程如下:
探究过程如下:
1.连接实验装置并检查装置气密性
Ⅱ.向B中加入质量为m的铜锌合金粉末,由注射器A向B
缓缓加入稀硫酸,待B中不再有气体产生气体时,夹紧弹簧夹,
立即移出D中导管,准确读取并记录量筒内水的体积。
Ⅲ.经过滤等操作,准确称量并记录B中剩余固体物质的
质量。
IV.该小组的甲同学根据反应前后B中固体物质的质量计
算样品中锌的质量分数;乙同学认定量筒内测得水的体积
即为反应生成气体的体积,并利用该气体在常温下的密度,根据化学方程式进行相关计算,得到样品中锌的质量分数。
请回答下列问题:
(1) B中发生反应的化学方程式是
。
(2)Ⅲ中,正确的操作顺序是:过滤、 、 、称量。
(3)通过误差分析,化学小组发现乙同学所用数据不可靠。造成该数据不可靠的原因及其对计算结果的影响是:
①II中,移出D中的导管内留存有水,导致计算结果偏小。
② ,导致计算结果偏 。
……
13(1)Zn + H2SO4 == ZnSO4 + H2↑ (2)洗涤 干燥 (3)未考虑B中液体所占体积(或II中未待装置B冷却就读数D的数据等合理答案) 大

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
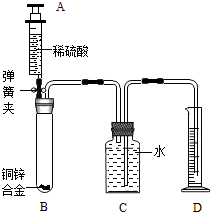 (2012?武汉)某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)
(2012?武汉)某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)

 ①II中,移出D中的导管内留存有水,导致计算结果偏小。
①II中,移出D中的导管内留存有水,导致计算结果偏小。