题目内容
融雪剂可以融化道路上的积雪。某种融雪剂由氯化钠和氯化钙组成,为测定该融雪剂中氯化钙的质量分数,称量2.4 g融雪剂放入烧杯中,加足量水使其完全溶解,再加入碳酸钠溶液至恰好完全反应,过滤后,将滤液蒸干得到2.46 g固体。求融雪剂中氯化钙的质量分数。
已知:Na2CO3 + CaCl2 === CaCO3↓ + 2NaCl
【解】设:2.4 g融雪剂中氯化钙的质量为x。
Na2CO3 + CaCl2 = CaCO3↓+ 2NaCl
|
x 2.46 g - (2.4 g - x)
|
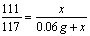
x = 1.11 g
|
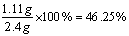
答:融雪剂中氯化钙的质量分数为46.25%。

练习册系列答案
相关题目


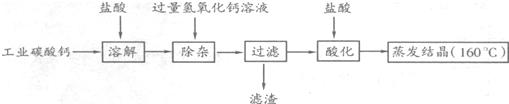
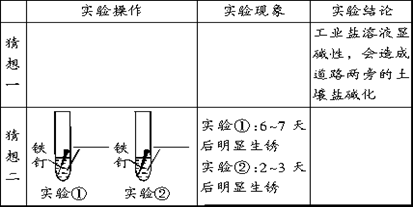 【反思与应用】 对于道路除冰,请你提出更好的建议___________________。
【反思与应用】 对于道路除冰,请你提出更好的建议___________________。