题目内容
为了测定某赤铁矿中三氧化二铁的质量分数,甲、乙两同学分别取该赤铁矿样品10g与足量的一氧化碳反应.甲同学将产生的气体通入足量的氢氧化钠溶液中,溶液的质量增加了6.6g;乙同学测得反应后固体的质量为7.6g.
(1)根据甲、乙两同学的实验数据分别计算该赤铁矿样品中三氧化二铁的质量;
(2)计算该赤铁矿样品中三氧化二铁的质量分数.
解:(1)甲同学实验生成CO2的质量为6.6 g
设含有Fe2O3的质量为x
Fe2O3+3C0 2Fe+3CO2
2Fe+3CO2
160 132
x 6.6g
x=8 g
乙同学实验中Fe2O3中氧元素的质量为10 g-7.6 g=2.4 g
所以Fe2O3的质量为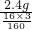 =8 g
=8 g
(2)由以上计算可知该赤铁矿中Fe2O3的质量分数为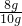 ×100%=80%
×100%=80%
答:(1)Fe2O3的质量为8 g.(2)赤铁矿样品中三氧化二铁的质量分数为80%.
分析:(1)根据题意,甲同学的实验可知:溶液增加的质量6.6g即一氧化碳还原氧化铁生成二氧化碳的质量,根据反应的化学方程式,由二氧化碳质量计算参加反应氧化铁的质量,
乙同学固体减少的量即是赤铁矿样品中氧元素的质量,而后依据化学式的计算可求氧化铁的质量;
(2)依据以上计算所得样品中氧化铁的质量完成赤铁矿样品中氧化铁的质量分数的计算;
点评:此题主要是在一氧化碳还原氧化铁的基础上考查有关化学方程式以及化学式的计算,注重学生综合能力的培养,是一道训练学生思维能力的综合题.
设含有Fe2O3的质量为x
Fe2O3+3C0
 2Fe+3CO2
2Fe+3CO2160 132
x 6.6g
x=8 g
乙同学实验中Fe2O3中氧元素的质量为10 g-7.6 g=2.4 g
所以Fe2O3的质量为
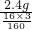 =8 g
=8 g(2)由以上计算可知该赤铁矿中Fe2O3的质量分数为
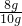 ×100%=80%
×100%=80%答:(1)Fe2O3的质量为8 g.(2)赤铁矿样品中三氧化二铁的质量分数为80%.
分析:(1)根据题意,甲同学的实验可知:溶液增加的质量6.6g即一氧化碳还原氧化铁生成二氧化碳的质量,根据反应的化学方程式,由二氧化碳质量计算参加反应氧化铁的质量,
乙同学固体减少的量即是赤铁矿样品中氧元素的质量,而后依据化学式的计算可求氧化铁的质量;
(2)依据以上计算所得样品中氧化铁的质量完成赤铁矿样品中氧化铁的质量分数的计算;
点评:此题主要是在一氧化碳还原氧化铁的基础上考查有关化学方程式以及化学式的计算,注重学生综合能力的培养,是一道训练学生思维能力的综合题.

练习册系列答案
相关题目