题目内容
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)在水、铜和氯化钠3种物质中,由分子构成的是________。
(2)食醋中含有醋酸(CH3COOH),醋酸由____种元素组成,1个分子中共有______个原子构成,其相对分子质量为_____,氢元素的质量分数为___(用计算式表示)
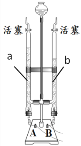
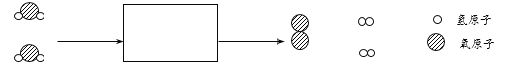
(3)用微观示意图表示工作舱中空气的主要成分,下图中最合理的是_____(填序号)。

【答案】水 3 8 60 ![]() ×100% C
×100% C
【解析】
(1)在水、铜、氯化钠3种物质中,因为水由分子构成,铜由原子构成,氯化钠由离子构成;
(2)醋酸是由碳、氢和氧三种元素组成的;一个醋酸分子是由2个碳原子、4个氢原子和2个氧原子构成的,则一个分子中共含有8个原子;醋酸的相对分子质量为12×2+1×4+16×2=60;醋酸中氢元素的质量分数=![]() ×100%=
×100%=![]() ×100%;
×100%;
(3)空气中氮气和氧气应该均匀分布,且氮气与氧气的体积比约为4:1。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。
(1)请写出镁条与氧气反应的化学方程式________________________________。
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律。我________(“同意”或“不同意”)小明的观点,因为___________________________。
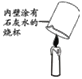
(3)小红按下图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。

(提出问题)黄色固体是什么呢?
(查阅资料)①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
(做出猜想)黄色固体是Mg3N2
(实验探究)请设计实验,验证猜想
实验操作 | 实验现象 | 结论 |
____________________ | _________ | _________ |
(反思与交流)空气中N2的含量计远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2 ,为什么呢?请给出合理的解释______________________________________。
(4)在化学实验中,影响化学反应速率的因素比较多。请以过氧化氢溶液制取氧气为例,设计实验探究影响化学反应速率的因素。
影响因素:___________
实验方案:____________________________________________________
实验结论:___________________________________________
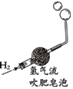
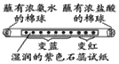
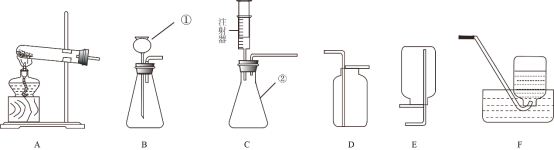
【题目】下列实验设计不能达到实验目的是( )
选项 | A | B | C | D |
实验设计 |
|
|
| 信息:氨水能使湿润 紫色石蕊试纸变蓝; 盐酸能使湿润紫色 石蕊试纸变红
|
实验 目的 | 红磷燃烧测定空气中氧气的含量 | 探究石蜡燃烧后有二氧化碳生成 | 验证氢气的密度比空气小 | 不同分子运动速率 |
A. A B. B C. C D. D