题目内容
29、实验室用锌粒和稀硫酸反应制取的氢气,经过净化干燥后,还原氧化铜.
(1)根据所得到铜粉的质量,可求得参加反应的氢气的质量,进而计算出应消耗的锌粒和稀硫酸的质量.但实际耗用的锌粒(不含杂质)和稀硫酸的质量都远远超过理论值.从实验过程看,可能的原因有哪些?(至少答出三点原因) ①
②
(2)Cu+在酸性溶液中不稳定,可发生反应生成Cu2+和Cu.Cu与强氧化性酸反应可得到铜盐溶液.现有浓硫酸、浓硝酸、稀硫酸、稀硝酸,而没有其他试剂.Cu2O是一种红色固体,如何用最简便的实验方法来检验经氢气还原CuO所得到的红色产物中是否含有Cu2O.
(1)根据所得到铜粉的质量,可求得参加反应的氢气的质量,进而计算出应消耗的锌粒和稀硫酸的质量.但实际耗用的锌粒(不含杂质)和稀硫酸的质量都远远超过理论值.从实验过程看,可能的原因有哪些?(至少答出三点原因) ①
氧化铜加热前要先通氢气,排去试管内空气
②
反应后热铜粉还需在氢气中冷却
③部分氢气通过装有氧化铜的试管时,未与氧化铜反应
(2)Cu+在酸性溶液中不稳定,可发生反应生成Cu2+和Cu.Cu与强氧化性酸反应可得到铜盐溶液.现有浓硫酸、浓硝酸、稀硫酸、稀硝酸,而没有其他试剂.Cu2O是一种红色固体,如何用最简便的实验方法来检验经氢气还原CuO所得到的红色产物中是否含有Cu2O.
取红色固体少量于试管中,向试管中滴加稀硫酸,充分振荡,若发现溶液变为蓝色,则说明样品中混有Cu2O,若没有发现溶液变为蓝色,则说明样品中没有Cu2O
.分析:(1)根据氢气还原氧化铜的步骤和注意事项回答;
(2)在验证是否有Cu2O时,可用利用Cu2O+H2SO4=CuSO4+Cu+H2O,若在红色固体中加入硫酸,出现蓝色溶液说明有氧化亚铜,否则没有.
(2)在验证是否有Cu2O时,可用利用Cu2O+H2SO4=CuSO4+Cu+H2O,若在红色固体中加入硫酸,出现蓝色溶液说明有氧化亚铜,否则没有.
解答:解:(1)在氢气还原氧化铜时,实验所用的氢气质量远远超过理论值,即实际耗用的锌粒(不含杂质)和稀硫酸的质量都远远超过理论值,原因主要是加热前要先通氢气,排去试管内空气,以防止氢气与空气混合加热发生爆炸;反应后热铜粉还需在氢气中冷却,以防止制得的铜又被氧化,这两部分氢气都不能与氧化铜反应而白白消耗掉;另外如果氢气通过的速度过快,可能会来不及与氧化铜充分反应而浪费.
(2)根据题中信息,可用利用反应Cu2O+H2SO4=CuSO4+Cu+H2O来检验,取红色固体少量于试管中,向试管中滴加稀硫酸,充分振荡,若发现溶液变为蓝色,则说明样品中混有Cu2O,若没有发现溶液变为蓝色,则说明样品中没有Cu2O.
故答案为:(1)①氧化铜加热前要先通氢气,排去试管内空气;②反应后热铜粉还需在氢气中冷却;③部分氢气通过装有氧化铜的试管时,未与氧化铜反应;
(2)取红色固体少量于试管中,向试管中滴加稀硫酸,充分振荡,若发现溶液变为蓝色,则说明样品中混有Cu2O,若没有发现溶液变为蓝色,则说明样品中没有Cu2O.
(2)根据题中信息,可用利用反应Cu2O+H2SO4=CuSO4+Cu+H2O来检验,取红色固体少量于试管中,向试管中滴加稀硫酸,充分振荡,若发现溶液变为蓝色,则说明样品中混有Cu2O,若没有发现溶液变为蓝色,则说明样品中没有Cu2O.
故答案为:(1)①氧化铜加热前要先通氢气,排去试管内空气;②反应后热铜粉还需在氢气中冷却;③部分氢气通过装有氧化铜的试管时,未与氧化铜反应;
(2)取红色固体少量于试管中,向试管中滴加稀硫酸,充分振荡,若发现溶液变为蓝色,则说明样品中混有Cu2O,若没有发现溶液变为蓝色,则说明样品中没有Cu2O.
点评:了解氢气还原氧化铜实验的实验步骤和注意事项是解决该类问题的关键,此外,氧化铜是一种黑色固体而氧化亚铜是红色.氧化铜中铜为+2价,而氧化亚铜中铜为+1价,所以在与硫酸反应时的现象不同.

练习册系列答案
相关题目
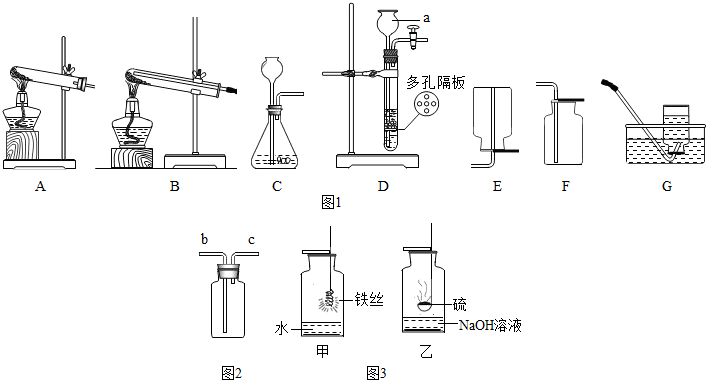
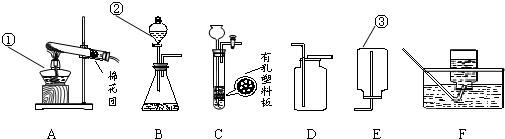
结合图示实验装置,回答下列问题.
(1)写出图中标号仪器的名称① ;② ;③ .
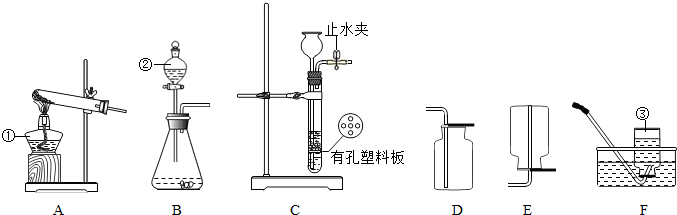
(2)实验室用锌粒和稀硫酸制取氢气的化学方程式为: .
若用C装置制取氢气,检查气密性的方法是 ,要想使该装置能更有效地达到控制反应的发生和停止,应将锌粒放在有孔塑料板的 (填“上面”或“下面”),其原理是 .
(3)实验室常用加热氢氧化钙固体和氯化铵固体混合物的方法来制取氨气,已知氨气的密度小于空气,易溶于水且能和水反应.则实验室制取氨气的发生装置为 (填字母编号,下同),收集装置为 .
(4)实验室用二氧化锰催化双氧水制取氧气,发生装置为 (从“A、B”中选择),收集装置为 ,反应的化学方程式为: .
(5)某化学兴趣小组同学想探究FeCl3溶液是否对过氧化氢的分解具有催化作用.
①请你帮助他们完成实验报告:
②经分析知:FeCl3溶液中存在H20、Fe3+和Cl-三种微粒,于是同学们提出了以下猜想:
甲同学:催化分解H202的是FeCl3溶液中的H20;
乙同学:催化分解H202的是FeCl3溶液中的Fe3+;
丙同学:催化分解H202的是FeCl3溶液中的Cl-.
你认为最不可能的是 同学的猜想,理由是 .
③同学们对余下的两个猜想,用实验进行了探究.请你仔细分析后填表:
(1)写出图中标号仪器的名称①

(2)实验室用锌粒和稀硫酸制取氢气的化学方程式为:
若用C装置制取氢气,检查气密性的方法是
(3)实验室常用加热氢氧化钙固体和氯化铵固体混合物的方法来制取氨气,已知氨气的密度小于空气,易溶于水且能和水反应.则实验室制取氨气的发生装置为
(4)实验室用二氧化锰催化双氧水制取氧气,发生装置为
(5)某化学兴趣小组同学想探究FeCl3溶液是否对过氧化氢的分解具有催化作用.
①请你帮助他们完成实验报告:
| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加5%的H202溶液,然后滴人适量的FeCl3溶液,把带火星的木条伸入试管. | FeCl3溶液可以 催化分解H202 |
甲同学:催化分解H202的是FeCl3溶液中的H20;
乙同学:催化分解H202的是FeCl3溶液中的Fe3+;
丙同学:催化分解H202的是FeCl3溶液中的Cl-.
你认为最不可能的是
③同学们对余下的两个猜想,用实验进行了探究.请你仔细分析后填表:
| 实验过程 | 实验现象 | 结论 |
| 向盛有5%的H202溶液的试管中加入少量的盐酸(含有Cl-),并把带火星的木条伸人试管. | 无明显现象 | |
| 向盛有5%的H202溶液的试管中加入少量的Fe2(S04)3溶液(含有Fe3+),并把带火星的木条伸人试管. |