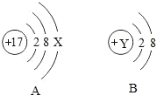
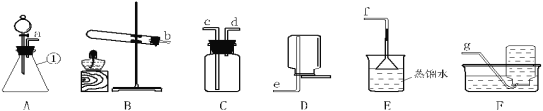题目内容
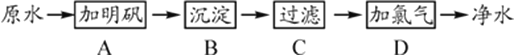
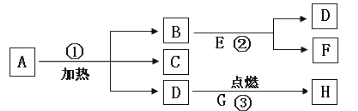
【题目】化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合下列实验装置图回答问题
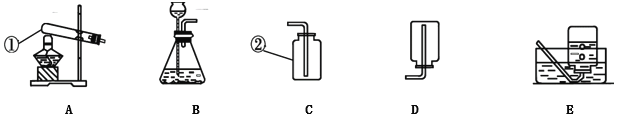
(1)写出指定仪器的名称:①_____;②_____。
(2)写出实验室中用过氧化氢溶液、高锰酸钾两种途径制取氧气的化学方程式_____、_____.
(3)实验室用高锰酸钾制取氧气时,可选用的发生装置是_____(填字母代号)。选用该装置的理由是_____;可用E装置收集氧气的依据是_____;实验结束时,某同学发现水槽中的水变成了浅紫红色,从实验操作角度分析其原因是_____。
(4)用B装置制取氧气长颈漏斗伸入面下的原因_____。
(5)实验室制取H2是用固态的锌粒和液态的稀硫酸在常温下反应进行的,可选用的气体发生装置是_____(填写装置序号),可以用D或E装置收集H2,说明H2具有_____、_____等性质。
【答案】试管 集气瓶 ![]()
![]() A 固体加热 氧气不易溶于水 试管口没放一团棉花 防止生成的气体从长颈漏斗下端管口逸到空气中 B 密度比空气小 难溶于水
A 固体加热 氧气不易溶于水 试管口没放一团棉花 防止生成的气体从长颈漏斗下端管口逸到空气中 B 密度比空气小 难溶于水
【解析】
过氧化氢溶液在二氧化锰催化作用下生成水和氧气,高锰酸钾加热分解生成锰酸钾和二氧化锰和氧气,氧气密度比空气大,不易溶于水,用排水法或向上排空气法收集,锌和稀硫酸反应生成硫酸锌和氢气,氢气不溶于水,密度比空气小,用向下排空气法或排水法收集。
(1)仪器的名称:①试管;②集气瓶。
(2)实验室中用过氧化氢溶液分解产生水和氧气,反应的化学方程式为![]() ,高锰酸钾加热分解生成锰酸钾和二氧化锰和氧气,化学方程式为
,高锰酸钾加热分解生成锰酸钾和二氧化锰和氧气,化学方程式为![]() 。
。
(3)实验室用高锰酸钾加热制取氧气时,可选用的发生装置是A。选用该装置的理由是高锰酸钾制取氧气要加热,属于固体加热型;可用E装置收集氧气的依据是氧气不易溶于水;实验结束时,某同学发现水槽中的水变成了浅紫红色,原因是试管口没放一团棉花,高锰酸钾粉末进入了水槽。
(4)用B装置制取氧气长颈漏斗伸入面下的原因防止生成的气体从长颈漏斗下端管口逸到空气中。
(5)实验室制取H2是用固态的锌粒和液态的稀硫酸在常温下反应生成氯化锌和氢气,可选用的气体发生装置是B,可以用D或E装置收集,说明![]() 具有密度比空气小、难溶于水等性质。
具有密度比空气小、难溶于水等性质。

 名校课堂系列答案
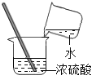
名校课堂系列答案【题目】萱萱同学在实验室发现了一瓶久置的标签残缺的无色溶液(如图甲所示),为确认中的溶质,他设计并进行了如下探究活动,请回答下列问题。
(猜想与假设)同学们在跟实验员老师了解了情况以后,猜想其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
(查阅资料)上述四种物质的相关信息如下:
物 质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
(探究实验)
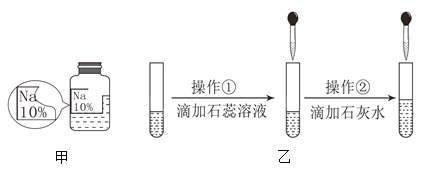
(1)通过查阅资料,他认为可以排除________________,依据是______________________。
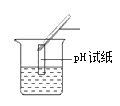
(2)他又做了如图乙所示实验继续探究,在进行操作①后可确定溶质不是NaCl,则其实验现象是________________________。
(3)在进行操作②时有白色沉淀产生,由此又可以排除猜想中的_______________,产生沉淀的反应的化学方程式是_______________________。(探究结论)该同学经过分析后认为标签也可能是“NaOH”,他的理由是_____________。另有同学猜想其中的溶质还可能是NaNO3,但萱萱同学通过对实验现象的分析否定了这种猜想,她的理由是___________________________________________________。
【题目】钙片的标签如图所示,且钙片中只有碳酸钙中含有钙元素。为测定其真实的含钙量,小东取10片钙片放入盛足量盐酸的烧杯中,充分反应后再称取烧杯和剩余物的总质量。
小东做了三次实验,数据如下表:
物质的质量/ g | 第一次 | 第二次 | 第三次 | 平均值 |
反应前:烧杯+盐酸 | 22 | 22 | 22 | 22 |
10片钙片 | 8 | 8 | 8 | 8 |
反应后:烧杯+剩余物 | 26.7 | 26.5 | 26.9 | 26.7 |
(1)请列式计算每片此钙片含碳酸钙的质量_______。
(2)请通过计算说明此标签中的含钙量是否合理_______。