��Ŀ����
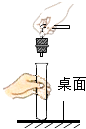
����Ŀ����ѧ��ȤС��������ͼ��ʾװ�ã��ⶨij̼��������CO2�ĺ����� 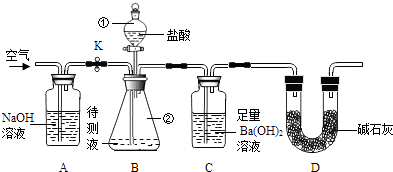
���ϣ���CO2������Ba��OH��2��Ӧ����BaCO3��������NaHCO3�����ᷴӦ����CO2
��һƿ�������24Сʱ��δ������������ȡһ������Ʒ���뵽ʢ�й���NaOH��Һ�������У���ַ�Ӧ��������Һ��
�ش��������⣺
��1��װ��B�������٢ڵ����Ʒֱ�Ϊ�� �� �����������ᣬ�������з����Ļ�ѧ��Ӧ����ʽΪ����
��2����Ӧ���������ͨ���������ȱ��װ��A����ʵ�������ƫ����ƫС������Ӱ�족����ͬ����������δ��أ���ʵ���� ��
��3��װ��D�������� �� ������¶ȹ��ͣ����Ͻ������ʵ��������ƫС�����ܵ�ԭ���� �� �����ⶨC��BaCO3��������ֻ�ⶨC��ʵ��ǰ����������ʵ��������ƫ�ߣ�ԭ���� ��
��4�����и����ʩ�У��������ʵ����ȷ�ȵ��� �� ������ĸ�� a���μ�����˹���
b����A��B֮������ʢ��Ũ�����ϴ��װ��
c����B��C֮������ʢ��NaHCO3��ϴ��װ�ã�
���𰸡�
��1����Һ©������ƿ
��2��ƫ��ƫС
��3����ֹ�����еĶ�����̼����Cװ�ã����Ͻ��������̼�ڱ�ˮ�е��ܽ������½���B��ˮ�������Ȼ�������Ƚ���Cװ��
��4��b��c
���������⣺��1����Һ©�������Һ��ҩƷ����ƿ�dz��õķ�Ӧ�������������ƺ����ᷴӦ�����Ȼ��ƺ�ˮ��̼���ƺ����ᷴӦ�����Ȼ��ƺ�ˮ�Ͷ�����̼����ƽ���ɣ����Դ��ǣ���Һ©������ƿ��NaOH+HCl=NaCl+H2O��Na2CO3+2HCl=2NaCl+H2O+CO2������NaHCO3+HCl=NaCl+H2O+CO2������2����Ӧ���������ͨ���������ȱ��װ��A����ʵ����ƫ����Ϊ�������ж�����̼��������δ��أ���ʵ����ƫС����Ϊ������ܽ�����¶ȳɷ��ȣ����Դ��ǣ�ƫ��ƫС��3��װ��D�������ǣ���ֹ�����еĶ�����̼����Cװ�ã�������¶ȹ��ͣ����Ͻ������ʵ��������ƫС�����ܵ�ԭ���ǣ����Ͻ��������̼�ڱ�ˮ�е��ܽ������½���B��ˮ�������Ȼ�������Ƚ���Cװ�ã����ֻ�ⶨC��ʵ��ǰ����������ʵ��������ƫ�ߣ����Դ��ǣ���ֹ�����еĶ�����̼����Cװ�ã����Ͻ��������̼�ڱ�ˮ�е��ܽ������½���B��ˮ�������Ȼ�������Ƚ���Cװ�ã���4����������ĵμ��ٶȣ��������ȷ�ȣ��������ʵ����ȷ�ȵ��ǣ���A��B֮������ʢ��Ũ�����ϴ��װ�ã���B��C֮������ʢ��NaHCO3��ϴ��װ�ã���Ϊa�������̼�����ٶȼ�����Cװ�����ն�����̼�����ף��ܹ���߽��ȷ�ȣ�b���A��B֮������ʢ��Ũ�����ϴ��װ�ã���������ˮ���������ǶԽ��û��Ӱ�죻c���B��C֮������ʢ��NaHCO3��ϴ��װ�ã���B�лӷ����Ȼ���������ϴ��װ���е�NaHCO3��Ӧ�����ɶ�����̼��ʹ�ⶨ���ƫ�ߣ����Դ��ǣ�b��c
�����㾫�����������⣬������Ҫ�˽���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ(ע�⣺a����ƽ b������ c������)��

 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�����Ŀ����һ��ҵ���̣���ʯ��CaC2�� ![]() �ҽ�
�ҽ� ![]() ���� ���е�ʯ��ˮ�ķ�ӦΪ��CaC2+2H2O=Ca��OH��2+C2H2��
���� ���е�ʯ��ˮ�ķ�ӦΪ��CaC2+2H2O=Ca��OH��2+C2H2��
��1����������Ҫ�ɷ���Ca��OH��2�� �� ��ҵ��������Ȳ��C2H2�������Ļҽ��Ͳ����Ʊ�����ԭ��KClO3�ͳ�ϸCaCO3 ��
��2�����Ʊ�KClO3���������£� 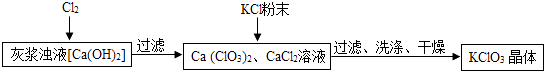
��ҽ���Һ��ͨ��Cl2 �� �õ�Ca��ClO3��2��CaCl2��Һ����Ӧ��Ca��ClO3��2��CaCl2�Ļ�ѧ�������ֱ�Ϊ1��5��д���˷�Ӧ�Ļ�ѧ����ʽ ��
��3���й������ڳ����µ��ܽ�����£�
���� | Ca��ClO3��2 | CalO3 | KClO3 | KCl |
�ܽ��/g | 209.0 | 74.5 | 7.3 | 34.2 |
���������м���KCl��ĩ��KCl�����ѧʽ�������˸��ֽⷴӦ���õ�KClO3���壮����Ϊ�ܵõ�KClO3�����ԭ���� ��
��4��ϴ��ʱ����ѡ������ϴ�Ӽ�������ĸ��ţ��� A��KCl������Һ B����ˮ C������KClO3��Һ
��5�����Ʊ���ϸCaCO3���������£�ע������NH4Cl��Ŀ�����ܽ�����е������Σ��� 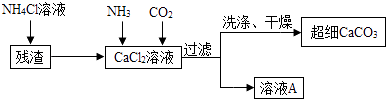
��CaCl2��Һ��ͨ���������壬���ɳ�ϸCaCO3�Ļ�ѧ����ʽ ��
��6����������ҺA��ѭ��ʹ�ã�����Ҫ�ɷֵĻ�ѧʽ�� ��
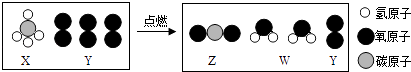
����Ŀ��һ�������£���һ�ܱյ������з���ij��Ӧ����÷�Ӧ�����и����ʵ��������±���ʾ��
���� | X | Y | Z | Q |
��һ�β�õ�����/g | 32 | 51 | ©�� | 6 |
�ڶ��β�õ�����/g | 60 | 17 | 11 | 12 |
�����ж���ȷ���ǣ� ��
A.�÷�Ӧ��X��Q�������仯֮��Ϊ5��1
B.�÷�Ӧ�Ļ�ѧ����ʽ�ɱ�ʾΪ��Y��X+Z+Q
C.Z�����Ǹ÷�Ӧ�Ĵ���
D.�÷�Ӧ�������û���Ӧ