题目内容
【题目】锶元素的原子结构示意图和在元素周期表中显示的信息如图所示:
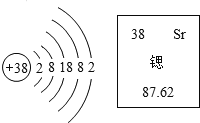
(1)锶属于______元素(填“金属”或“非金属”)。
(2)锶元素的原子序数为___________________。
(3)氧化锶的化学式是_____________,氧化锶与水能发生化合反应生成氢氧化锶并放出大量热,请你写出反应的化学方程式_____________。
【答案】金属 38 SrO SrO+H2O=Sr(OH)2
【解析】
(1)锶的名称中含有金字旁,属于金属元素;
(2)根据元素周期表中的信息可知,位于左上角的数字表示原子序数,即核电荷数和质子数,所以锶元素的原子序数为38;
(3)锶元素的最外层电子数为2,易失去两个电子而带两个单位的正电荷,故氧化锶的化学式为SrO;氧化锶与水能发生化合反应生成氢氧化锶,反应的化学方程式为SrO+H2O=Sr(OH)2。

【题目】下列实验方案能达到实验目的的是
选项 | A | B | C | D |
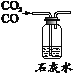
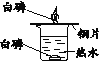
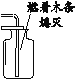
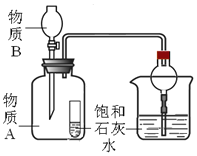
实验目的 | 证明CO2可与H2O反应生成H2CO3 | 除去CO2中的少量CO | 证明可燃物燃烧需要与O2接触 | 证明集气瓶中已充满CO2 |
实验方案 |
|
|
|
|
A. A B. B C. C D. D
【题目】下表提供了硝酸钾固体在不同温度时的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(1)20℃时,向50 g水中加入20 g硝酸钾,充分溶解后得到__________(选填:饱和或不饱和)溶液,溶液的溶质质量分数为_________(保留一位小数)。
(2)现有60℃时的硝酸钾饱和溶液210 g,若降温至20℃,析出硝酸钾晶体的质量是____,通过________操作可将析出的硝酸钾晶体和溶液分离。
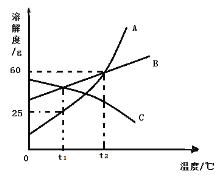
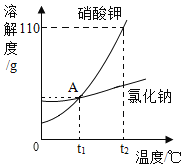
(3)现有80℃时溶质质量分数为30%的硝酸钾溶液,则降温到________(填字母)能得到硝酸钾针状晶体。
a. 0℃-20℃ b. 20℃-40℃ c. 40℃-60℃ d. 60℃-80℃
(4)用100g10%的硝酸钾溶液配制5%的硝酸钾溶液。需要加水_______亳升(水的密度为1.0g·mL-1)
【题目】学习《海水“制碱”》的知识后,小明在实验室中进行了如下探究活动,请你和小明一起完成下面的实验探究活动。
(1)探究碳酸钠的溶解性:在编号为 A、B、C、D 的四个烧杯中各加入室温下的水 100g,并分别加入取自实验室的碳酸钠固体,搅拌至充分溶解,实验数据记录如下表:
烧杯编号 | A | B | C | D |
水的质量/g | 100 | 100 | 100 | 100 |
加入 Na2CO3 的质量/g | 30 | 35 | 40 | 50 |
溶液的质量/g | 130 | 135 | 140 | 140 |
分析上述数据,烧杯编号为_________中的溶液是饱和溶液。
(2)探究食用纯碱的纯度:小明把家中厨房里的食用纯碱(主要成分是Na2CO3)带到实验室,他称取食用纯碱12.0g放入烧杯中,加入200g水使其完全溶解。现将150g一定浓度的CaCl2溶液逐滴滴入烧杯中,测得滴加氯化钙溶液的质量与生成沉淀的质量关系如下表:
CaCl2 溶液的质量/g | 25 | 50 | 75 | 100 | 125 | 150 |
沉淀的质量/g | 2 | 4 | m | 8 | 10 | 10 |
①m 的数值是 ______。
②计算纯碱样品中碳酸钠的质量分数______(写出计算过程,计算结果保留一位小数)。
③滴加氯化钙溶液过量的目的是______。
【题目】某化学实验小组利用蜡烛进行了下列实验。
实验1:
序号 | 1-1 | 1-2 | 1-3 |
操作 |
|
|
|
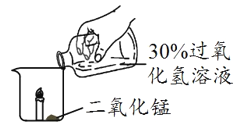
现象 | 燃烧的蜡烛保持原状 | 燃烧的蜡烛熄灭 | 剧烈反应,有大量气泡和水雾生成,燃烧的蜡烛熄灭了 |
(1)实验1-2中,燃烧的蜡烛熄灭的原因是____。
(2)实验1-3中,反应生成氧气的化学方程式为___。
实验2:
(提出问题)实验1-3中燃烧的蜡烛为什么会熄灭?
(猜想与假设)
I.蜡烛燃烧生成的二氧化碳导致其熄灭。
II.过氧化氢分解时吸收热量,蜡烛周围的温度降低到着火点以下,导致其熄灭。
III.过氧化氢分解产生的水雾导致蜡烛熄灭。
(进行试验)
序号 | 2-1 | 2-2 | 2-3 |
操作 |
|
|
|
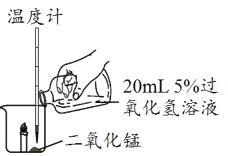
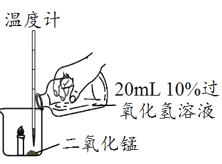
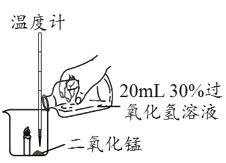
现象 | 有气泡产生,蜡烛火焰无明显变化,温度升高不明显 | 有较多气泡和少量水雾产生,蜡烛燃烧更旺。火焰明亮,温度升高较明显 | 剧烈反应,有大量气泡和水雾产生,燃烧的蜡烛熄灭,温度升高明显 |
(解释与结论)
(3)甲同学认为猜想I不成立,他的依据是____。
(4)通过实验验证,可以得出猜想____(填序号)成立。
(5)上述实验中,能证明氧气有助燃性的实验及现象是____。
(反思与评价)
(6)依据上述实验,若保持实验1-3中蜡烛不熄灭,可采用的方法有___。