题目内容
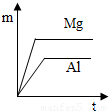
室温下,等质量的镁片和铝片分别与足量的稀硫酸反应,产生氢气的质量(m)与时间(t)的关系图正确的是( )
A、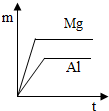 | B、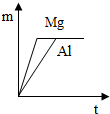 | C、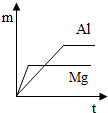 | D、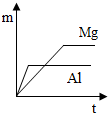 |
分析:根据金属的活动性镁>铝,镁与稀硫酸反应比铝剧烈,相同时间内镁与稀硫酸反应放出氢气质量大于铝;
根据金属与足量稀硫酸反应放出氢气的质量=
×金属质量,等质量的镁片和铝片与足量稀硫酸反应,所放出氢气的质量大小取决于两金属的化合价与相对原子质量的比;据此可判断等质量铝完全反应放出氢气质量大量镁片.
根据金属与足量稀硫酸反应放出氢气的质量=
| 金属化合价 |
| 金属的相对原子质量 |
解答:解:由于金属镁的活动性大于铝,在相同时间内镁片所放出氢气的质量大于铝片;据此可判断图D错误;
假设两种金属的质量为m,则与足量稀硫酸完全反应放出氢气的质量分别为:
镁完全反应产生氢气的质量=
× m=
;
铝完全反应产生氢气的质量=
×m=
.
因为
<
,所以等质量镁与硫酸完全反应所产生氢气质量小于铝;据此可判断图A、图B错误;
故选C.
假设两种金属的质量为m,则与足量稀硫酸完全反应放出氢气的质量分别为:
镁完全反应产生氢气的质量=
| 2 |
| 24 |
| m |
| 12 |
铝完全反应产生氢气的质量=
| 3 |
| 27 |
| m |
| 9 |
因为
| m |
| 12 |
| m |
| 9 |
故选C.
点评:根据金属活动性可判断金属与酸反应的剧烈程度;根据金属与足量酸完全反应放出氢气质量可判断,等质量的金属完全反应放出氢气质量的大小;此类问题多由这两个方面进行判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目