题目内容
实验室有一包白色粉末状物质,可能由KCl、Na2SO4、Na2CO3、CuSO4中的一种或几种组成.为了确定原粉末的成分,某校化学兴趣小组的小妍同学,按如图所示进行实验:
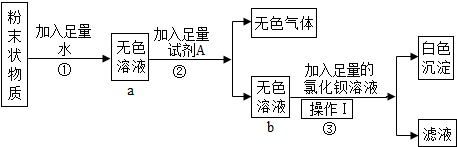
请回答下列问题:
(1)粉末中一定不含 ,操作Ⅰ的名称是 .
(2)为了不干扰对下一步实验现象的判断,试剂A最好选择什么试剂?写出步骤③中发生反应的化学方程式.

请回答下列问题:
(1)粉末中一定不含
(2)为了不干扰对下一步实验现象的判断,试剂A最好选择什么试剂?写出步骤③中发生反应的化学方程式.
考点:物质的鉴别、推断,过滤的原理、方法及其应用,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:混合物组成的推断题
分析:根据硫酸铜在溶液中显蓝色,硫酸根离子和钡离子会生成不溶于酸的硫酸钡沉淀,碳酸根离子和钡离子会生成溶于酸的碳酸钡沉淀等知识进行分析.
解答:解:硫酸铜在溶液中显蓝色,硫酸根离子和钡离子会生成不溶于酸的硫酸钡沉淀,碳酸根离子和钡离子会生成溶于酸的碳酸钡沉淀.
加入足量的水得到无色溶液,硫酸铜在溶液中显蓝色,所以白色粉末状物质一定没有CuSO4,加入A有无色气体,说明A是酸,一定有碳酸钠,因为碳酸钠与氯化钙不能共存,因此一定没有氯化钙;为了不干扰对下一步实验现象的判断,试剂A最好选择硝酸;加入足量的氯化钡溶液,有白色沉淀生成,说明一定有硫酸钠;若要检验KCl是否存在,可采用的方法是:先加稀硝酸进行酸化,再加硝酸银溶液,观察是否有白色沉淀生成,所以
(1)通过推导可知,粉末中一定不含硫酸铜,经过操作Ⅰ后,得到了白色沉淀和滤液,所以操作Ⅰ是过滤;
(2)为了不干扰对下一步实验现象的判断,试剂A最好选择硝酸,步骤③中发生的反应是氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,化学方程式为:BaCl2+Na2SO4═BaSO4↓+2NaCl.
故答案为:(1)CuSO4,过滤;
(2)硝酸,BaCl2+Na2SO4═BaSO4↓+2NaCl.
加入足量的水得到无色溶液,硫酸铜在溶液中显蓝色,所以白色粉末状物质一定没有CuSO4,加入A有无色气体,说明A是酸,一定有碳酸钠,因为碳酸钠与氯化钙不能共存,因此一定没有氯化钙;为了不干扰对下一步实验现象的判断,试剂A最好选择硝酸;加入足量的氯化钡溶液,有白色沉淀生成,说明一定有硫酸钠;若要检验KCl是否存在,可采用的方法是:先加稀硝酸进行酸化,再加硝酸银溶液,观察是否有白色沉淀生成,所以
(1)通过推导可知,粉末中一定不含硫酸铜,经过操作Ⅰ后,得到了白色沉淀和滤液,所以操作Ⅰ是过滤;
(2)为了不干扰对下一步实验现象的判断,试剂A最好选择硝酸,步骤③中发生的反应是氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,化学方程式为:BaCl2+Na2SO4═BaSO4↓+2NaCl.
故答案为:(1)CuSO4,过滤;
(2)硝酸,BaCl2+Na2SO4═BaSO4↓+2NaCl.
点评:在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2013年初,京津冀地区遭遇大范围长时间的雾霾天气.大自然再次为我们敲响环保警钟.以下有关环境保护的叙述中错误的是( )
| A、乱扔塑料袋、泡沫快餐盒会造成“白色污染” |
| B、城市的能见度较低,主要是烟雾和粉尘污染所致 |
| C、公园里大理石雕像被腐蚀,这是温室效应所致 |
| D、不合格装饰材料中,常含甲醛、苯等致癌物,会污染室内环境 |