题目内容
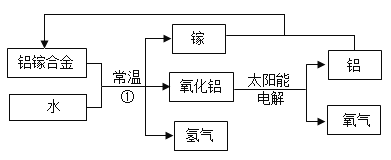
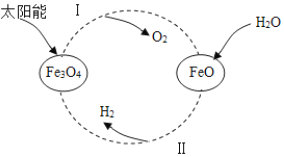
【题目】目前入们使用的燃料大多来自化石燃料,如______、石油、天然气等。天然气的主要成分是甲烷(CH4),甲烷完全燃烧的化学方程式是______,氢能是理想的清洁能源。以太阳能为热源,经由铁氧化合物循环分解水的过程如图所示。
(1)反应1的基本反应类型为______。
(2)写出在一定条件下发生的反应Ⅱ的化学方程式______。
(3)在上述循环过程中,最终得到的产品是______和______。
【答案】煤 CH4+2O2![]() CO2+2H2O 分解反应 3FeO+H2O
CO2+2H2O 分解反应 3FeO+H2O![]() Fe3O4+H2 H2 Fe3O4
Fe3O4+H2 H2 Fe3O4
【解析】
人类使用的化石燃料主要是煤、石油和天然气,故填煤;反应物是甲烷和氧气,生成物是二氧化碳和水,方程式故填CH4+2O2![]() CO2+2H2O;
CO2+2H2O;
(1)由图可知,反应I为四氧化三铁在太阳能的作用下发生反应生成氧化亚铁和氧气,属于分解反应,故填分解反应;
(2)由图可知过程Ⅱ的化学方程式是氧化亚铁与水蒸气反应生成四氧化三铁和氢气,反应中水是气态,反应方程式为3FeO+H2O![]() Fe3O4+H2,故填3FeO+H2O
Fe3O4+H2,故填3FeO+H2O![]() Fe3O4+H2;
Fe3O4+H2;
(3)由图可知在上述循环过程中,最终得到的产品有氢气,故填H2(或氢气);还有四氧化三铁,故填Fe3O4(或四氧化三铁)。

 快捷英语周周练系列答案
快捷英语周周练系列答案【题目】同学们学习了燃烧与灭火的相关知识后,进行了下列探究实验:
(实验探究)
步骤 | 实验操作 | 实验现象 | 结论或解释 |
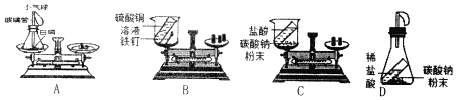
(1) | 用玻璃棒分别蘸取95%的酒精(C2H5OH)、蒸馏水置于火焰上。 | 酒精燃烧, 蒸馏水不燃烧。 | 结论:酒精是可燃物,水不是可燃物。写出酒精燃烧的化学方程式:_____。 |
(2) | 在铁片两端放大小相同的硬纸片、乒乓球碎片,在铁片中间加热。 | 乒乓球碎片先燃烧、硬纸片后燃烧。 | 结论:乒乓球碎片的_____比硬纸片的低。 |
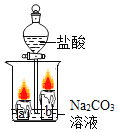
(3) | 在如图中打开分液漏斗的旋塞。
| ①溶液中产生气泡;②蜡烛火焰a_____(填“先于”“后于”) b熄灭。 | 现象②的原因是:CO2不助燃且不能燃烧:_____。 |
(4) | 用大烧杯罩住高低两支点燃的蜡烛。
| ①烧杯底部变黑; ②蜡烛火焰d比c先熄灭。 | 现象①的原因是:_____; 现象②的原因是:_____。 |
(拓展)堆积的面粉不容易点燃,即使少量点燃也只是小火燃烧;如果把面粉撒向空中遇火星可能会发生爆炸。“小火燃烧”的原因是:_____。