题目内容
【题目】图为某学习小组在白色点滴板上进行的有关“溶液的酸碱性”的探究实验。
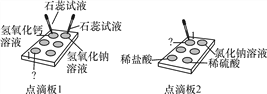
(1)使用白色点滴板进行实验的优点是________________________________(答一点)。
(2)稀盐酸和稀硫酸都能使紫色石蕊试液变红,是因为在不同酸的溶液中都含有相同的________(填微粒符号)。
(3)为了便于观察石蕊试液在酸碱性溶液中的颜色变化,在两块点滴板的1号空穴中,在滴加石蕊试液之前,都应该加________作为空白对照。
(4)点滴板2中的废液,若直接排入铸铁管下水道,会造成的危害是________________。
(5)你建议如何处理点滴板2中的废液。_______________________
【答案】 节约药品(或减少污染、现象明显、操作方便) H+ 蒸馏水 腐蚀铁管或导致污染 和点滴板1中的废液混合并调节溶液的pH为7后再排放
【解析】(1)根据使用白色点滴板进行实验的具体操作中出现的各种情况来分析其优点;
(2)根据酸的溶液中都存在的离子来分析其都能使紫色石蕊试液变红的原因;
(3)先证明不是石蕊溶液中的水使之变色;
(4)根据酸会与金属反应分析解答;
(5)根据中和反应的原理分析解答。
解:(1)使用白色点滴板进行实验,药品的用量少,则可节约药品,同时可减少对环境的污染,有时可以同时完成几个实验,便于观察比较;
(2)稀盐酸和稀硫酸都含有H+,具有相似的性质,所以稀盐酸和稀硫酸都能使紫色石蕊试液变红;
(3)为了便于观察石蕊试液在酸碱性溶液中的颜色变化,在两块点滴板的1号空穴中,在滴加石蕊试液之前,都应该加蒸馏水作为空白对照;
(4)酸会与金属反应而将铸铁下水道腐蚀或造成污染;
(5)用适量的碱性物质处理。故可和点滴板1中的废液混合并调节溶液的pH为7后再排放。