题目内容
【题目】根据如图所示的溶解度曲线,判断下列说法中不正确的是( ) 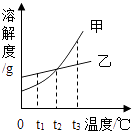
A.t1℃时,溶解度:甲<乙
B.t2℃时,甲乙两物质的饱和溶液溶质的质量分数相等
C.将t1℃时的乙饱和溶液升温到t2℃,所得溶液为饱和溶液
D.将t3℃甲、乙两种物质的饱和溶液,降温至t2℃,析出晶体的质量:甲>乙
【答案】C
【解析】解:A、由溶解度曲线可知:t1℃时,溶解度:甲<乙正确,正确但不符合题意,故选项错误;
B、t2℃时,甲乙两物质的饱和溶液溶质的质量分数相等正确,因为它们在该温度下有交点,正确但不符合题意,故选项错误;
C、将t1℃时的乙饱和溶液升温到t2℃,所得溶液为饱和溶液错误,升温后,乙变为不饱和溶液,错误符合题意,故选项正确;
D、将t3℃甲、乙两种物质的饱和溶液,降温至t2℃,析出晶体的质量:甲>乙,因为甲的溶解度随温度的升高变化比乙大,正确但不符合题意,故选项错误;
故选C
【考点精析】通过灵活运用饱和溶液和不饱和溶液相互转变的方法和固体溶解度曲线及其作用,掌握饱和和不饱和的转变方法:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低②最可靠的方法是:加溶质、蒸发溶剂;1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和)即可以解答此题.

【题目】Cu﹣Mg合金常用作飞机天线等导电材料.欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金8g放入烧杯,将200g稀H2SO4分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀H2SO4质量/g | 50 | 50 | 50 | 50 |
剩余固体质量/g | 6.8 | 5.6 | 4.6 | 4.6 |
(1)Cu﹣Mg合金中Cu的质量.
(2)求所加稀H2SO4的浓度.(写出计算过程)