题目内容
【题目】南昌大学研发的“硅衬底高光效GaN基蓝色发光二极管技术”获得2015年国家技术发明一等奖,请回答下列问题:
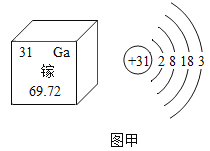
图乙
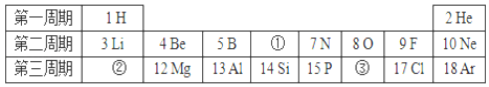
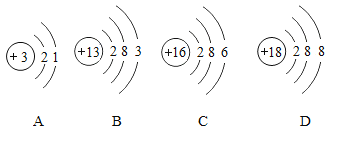
(1)图甲是镓在元素周期表中的信息以及原子结构示意图。镓的相对原子质量为:_____;如图乙原子结构示意图所对应的元素与镓元素的化学性质相似的是_____(填序号);
(2)图乙中属于金属元素的原子结构示意图是_____(填序号,下同)。达到稳定结构的粒子是_____。B和C两种元素的原子构成的化合物的化学式为_____。
(3)传统制备氮化镓的化学原理是: ,其中X的化学式为_____。
,其中X的化学式为_____。
【答案】69.72 B AB D Al2S3 HCl
【解析】
(1)图中元素周期表可以获得的信息,汉字下面的数字表示相对原子质量,镓的相对原子质量为69.72。元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,由题干中提供的乙原子结构示意图,镓原子的最外层电子数为3,则与其化学性质相似的粒子结构示意图中最外层电子数也应为3,B符合要求。故填:69.72;B。
(2)原子结构示意图中圆圈内数字代表质子数,又因在原子中质子数=原子序数,因此由图乙可确定各元素分别是锂、铝、硫、氩,金属元素除汞外都带金字旁,因此属于金属元素的原子是AB。若粒子的最外层电子数为8,属于相对稳定结构(一层时为2),图中D的最外层为电子数为8,属于相对稳定结构。B和C两种元素分别是铝、硫元素,形成的化合物是硫化铝,铝元素显+3价,硫元素显-2价,其化学式为:Al2S3。故填:AB;D;Al2S3。
(3)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反应前镓、氯、氮、氢原子个数分别为1、3、1、3,反应后的生成物中镓、氯、氮、氢原子个数分别为1、0、1、0,根据反应前后原子种类、数目不变,则3X分子中含有3个氢原子和3个氯原子,则每个X分子由1个氢原子和1个氯原子构成,则物质X的化学式为HCl。故填:HCl。

 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案【题目】小明同学在实验结束进行废液处理,将氢氧化钠、石灰水和稀盐酸倒入同一洁净的烧杯中,当他用手接触烧杯外壁时,感觉到“发热”,这一现象引起了他的注意,于是他进行了如下探究。
[提出问题]这三种物质混合后,溶液中溶质的组成有几种可能?这三种物质间发生反应的一个化学方程式为_____。你认为发热的原因是______。
[提出假设]小明对反应后溶液中溶质的组成作出了两种合理的假设。
假设①:溶质为NaCl、CaCl2
假设②:溶质为NaCl、CaCl2、 NaOH、 Ca(OH)2
假设③:溶质为NaCl、CaCl2、NaOH
请你再补充一种合理的假设
假设④:溶质为________。
[实验验证]如果假设④成立,请你设计一个实验方案进行验证。
实验步骤及操作方法 | 实验现象 | 实验结论 |
____ | ____ | 假设④成立 |
[实验反思] (1)比较几种假设,能说明作出假设④的理由是__。
(2)在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑_____。