题目内容
某同学想探究贝壳中碳酸钙的质量分数,取贝壳50g高温加热,完全反应后称量固体剩余物质量为32.4g,则贝壳中碳酸钙的质量分数
- A.90%
- B.95%
- C.80%
- D.70%
C
分析:根据碳酸钙高温分解生成氧化钙和二氧化碳,反应前后固体的质量差即为分解所放出二氧化碳的质量,由二氧化碳质量计算出50g贝壳中所含碳酸钙的质量,碳酸钙质量与贝壳质量比可计算贝壳中碳酸钙的质量分数.
解答:根据质量守恒定律,50g贝壳高温加热完全反应后放出二氧化碳的质量=50g-32.4g=17.6g
设贝壳中碳酸钙的质量为x
CaCO3 CaO+CO2↑
CaO+CO2↑
100 44
x 17.6g
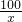 =
=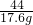 x=40g
x=40g
贝壳中碳酸钙的质量分数=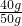 ×100%=80%
×100%=80%
故选C.
点评:根据化学方程式进行计算时,所使用的质量必须为纯净物的质量,由于题中剩余的32.4g固体物质可能含有杂质,因此,不能直接使用该质量进行计算.
分析:根据碳酸钙高温分解生成氧化钙和二氧化碳,反应前后固体的质量差即为分解所放出二氧化碳的质量,由二氧化碳质量计算出50g贝壳中所含碳酸钙的质量,碳酸钙质量与贝壳质量比可计算贝壳中碳酸钙的质量分数.
解答:根据质量守恒定律,50g贝壳高温加热完全反应后放出二氧化碳的质量=50g-32.4g=17.6g
设贝壳中碳酸钙的质量为x
CaCO3
 CaO+CO2↑
CaO+CO2↑100 44
x 17.6g
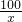 =
=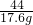 x=40g
x=40g贝壳中碳酸钙的质量分数=
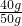 ×100%=80%
×100%=80%故选C.
点评:根据化学方程式进行计算时,所使用的质量必须为纯净物的质量,由于题中剩余的32.4g固体物质可能含有杂质,因此,不能直接使用该质量进行计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某同学想探究贝壳中碳酸钙的质量分数,取贝壳50g高温加热,完全反应后称量固体剩余物质量为32.4g,则贝壳中碳酸钙的质量分数( )
| A、90% | B、95% | C、80% | D、70% |