题目内容
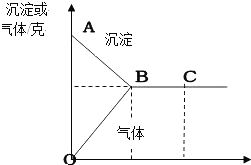 有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,现象如图所示(ABC表示沉淀变化,OBC表示气体变化)
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.取样溶于水,有白色沉淀产生;过滤后,向该白色沉淀中滴加盐酸,现象如图所示(ABC表示沉淀变化,OBC表示气体变化)(1)由此推断原白色固体中一定含有的是
(2)在C点时,所得溶液中的溶质一定有
考点:物质的鉴别、推断,碱的化学性质,盐的化学性质
专题:混合物组成的推断题
分析:(1)依据图象结合物质的性质进行分析,滴入盐酸沉淀会溶解,但是沉淀不会全部溶解,且有气体生成,据此解答即可.
(2)考虑各化学反应的反应产物.
(2)考虑各化学反应的反应产物.
解答:解:
(1)将固体溶解于水,硫酸钠会与氯化钡反应生成硫酸钡沉淀,硫酸钡不溶于盐酸;碳酸钠会与氯化钡反应生成碳酸钡沉淀,碳酸钡沉淀会溶于盐酸,据图可以看出,加入盐酸,沉淀减少,然后不变,且有气体生成,故一定含有碳酸钡沉淀和硫酸钡沉淀,所以混合物中一定含有碳酸钠、硫酸钠和氯化钡;
(2)因为硫酸钠会与氯化钡反应生成硫酸钡沉淀和氯化钠;碳酸钠会与氯化钡反应生成碳酸钡沉淀和氯化钠;碳酸钡沉淀会溶于盐酸生成二氧化碳和氯化钡、水,故在C点时,所得溶液中的溶质一定有氯化钠.
故答案为:
(1)碳酸钠、硫酸钠和氯化钡;
(2)氯化钠、氯化钡.
(1)将固体溶解于水,硫酸钠会与氯化钡反应生成硫酸钡沉淀,硫酸钡不溶于盐酸;碳酸钠会与氯化钡反应生成碳酸钡沉淀,碳酸钡沉淀会溶于盐酸,据图可以看出,加入盐酸,沉淀减少,然后不变,且有气体生成,故一定含有碳酸钡沉淀和硫酸钡沉淀,所以混合物中一定含有碳酸钠、硫酸钠和氯化钡;
(2)因为硫酸钠会与氯化钡反应生成硫酸钡沉淀和氯化钠;碳酸钠会与氯化钡反应生成碳酸钡沉淀和氯化钠;碳酸钡沉淀会溶于盐酸生成二氧化碳和氯化钡、水,故在C点时,所得溶液中的溶质一定有氯化钠.
故答案为:
(1)碳酸钠、硫酸钠和氯化钡;
(2)氯化钠、氯化钡.
点评:本题考查了混合物成分的推断,完成此题,可以依据图象结合物质的性质进行.

练习册系列答案
相关题目
下列基本操作正确的是( )
| A、用称量固体药品时,砝码放在左盘 |
| B、用量筒量液体时,视线应与量筒内凹液面最低处保持水平 |
| C、向试管中倾倒液体时,试剂瓶口与试管口可不接触 |
| D、用嘴吹灭酒精灯 |

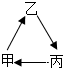 甲、乙、丙三种化合物均含有人体内最多的金属元素,它们之间存在如图所示的转化关系,其中甲是氧化物.
甲、乙、丙三种化合物均含有人体内最多的金属元素,它们之间存在如图所示的转化关系,其中甲是氧化物.