题目内容
图表是整理数据、发现其中规律的一种重要工具,1-18号元素原子最外层电子数与原子序数的关系如下图.试回答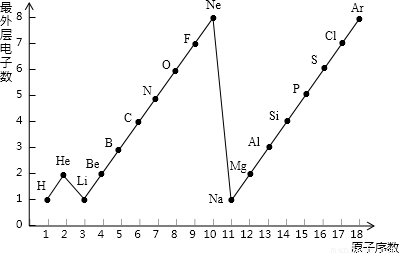
(1)第三周期11~18号元素原子最外层电子数变化的趋势是______.
(2)图中He与Ne,Ar原子最外层电子数不一样,但都处在每周期的结尾处,从原子的结构上分析其原因______.
(3)在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低探究钾元素(原子序数为19)单质与水反应的生成物,甲同学猜想生成物为KOH和H2,乙同学猜想生成物为KOH和O2,你认为______同学的猜想不合理,请从化合价的角度解释原因______.
【答案】分析:根据在元素周期表中,随原子序数的递增,原子结构中电子层数、最外层电子数发生规律性的变化,元素的种类(金属、非金属、稀有气体)和元素性质,也发生规律性的变化,解答本题.
解答:解:解:(1)在元素周期表中,随原子序数的递增,同一周期元素最外层电子数逐渐增多的规律,故答案为:逐渐递增(或从1到8逐渐递增);
(2)稀有气体元素的化学性质都是比较稳定的,一般不与其他物质发生化学反应,这与它们最外层电子数都是8(氦2个)的稳定结构有关,故答案为:已达到相对稳定结构
(3)在化学反应中,各元素在化合物里的正负化合价的代数和为零,元素的化合价有升有降,
故答案为:乙 只有化合价升高没有化合价降低了
点评:本题考查学生对元素周期表中的一些变化规律的归纳和总结,用化合价的知识解释化学反应,并学以致用.
解答:解:解:(1)在元素周期表中,随原子序数的递增,同一周期元素最外层电子数逐渐增多的规律,故答案为:逐渐递增(或从1到8逐渐递增);
(2)稀有气体元素的化学性质都是比较稳定的,一般不与其他物质发生化学反应,这与它们最外层电子数都是8(氦2个)的稳定结构有关,故答案为:已达到相对稳定结构
(3)在化学反应中,各元素在化合物里的正负化合价的代数和为零,元素的化合价有升有降,
故答案为:乙 只有化合价升高没有化合价降低了
点评:本题考查学生对元素周期表中的一些变化规律的归纳和总结,用化合价的知识解释化学反应,并学以致用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



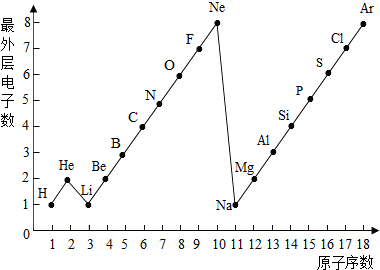 图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如右图.试回答:
图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如右图.试回答: 图表是整理数据.发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答:
图表是整理数据.发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答: