题目内容
 图表是整理数据.发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答:
图表是整理数据.发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答:(1)第三周期11一18号元素原子最外层电子 数变化的趋势是
最外层电子数依次递增
最外层电子数依次递增
.(2)图中He与Ne.Ar原子最外层电子数不一样,但都处在每周期的结尾处,从原子结构上分析其原因
都达到了相对稳定结构
都达到了相对稳定结构
.(3)原子的核外电子排布,特别是最外层的电子数目,与元素的化学性质有密切关系.

分析:(1)根据图示考虑最外层电子数的变化规律;(2)根据相对稳定结构最外层电子数的特点考虑;(3)根据最外层电子数多于4个易得到电子,少于4个易失去电子和化学式的书写方法考虑.
解答:解:(1)由图示可知11一18号元素原子最外层电子数依次增加1,所以最外层电子数依次递增;
(2)由一层电子排布的,为2个电子的属于相对稳定结构,由多层电子构成的,最外层电子数是8的是相对稳定结构,氦核外有2个电子,氖最外层有8个电子,氩最外层有8个电子,都达到了相对稳定结构;
(3)最外层电子数少于4个易失去电子,最外层电子数多于4个易得到电子,钠核内质子数是11,最外层电子数是1,易失去1个电子,由于钠元素显+1价,氯元素显-1价,正价在前,负价在后,十字交叉再约简,所以化学式是:NaCl.
故答案为:(1)最外层电子数依次递增;(2)都达到了相对稳定结构;(3)
(2)由一层电子排布的,为2个电子的属于相对稳定结构,由多层电子构成的,最外层电子数是8的是相对稳定结构,氦核外有2个电子,氖最外层有8个电子,氩最外层有8个电子,都达到了相对稳定结构;
(3)最外层电子数少于4个易失去电子,最外层电子数多于4个易得到电子,钠核内质子数是11,最外层电子数是1,易失去1个电子,由于钠元素显+1价,氯元素显-1价,正价在前,负价在后,十字交叉再约简,所以化学式是:NaCl.
故答案为:(1)最外层电子数依次递增;(2)都达到了相对稳定结构;(3)

点评:解答本题关键是要知道最外层电子数是8属于相对稳定结构(1个电子层的电子数是2);知道最外层电子数少于4个易失去电子,最外层电子数多于4个易得到电子,熟悉化学式的书写方法.

练习册系列答案
相关题目



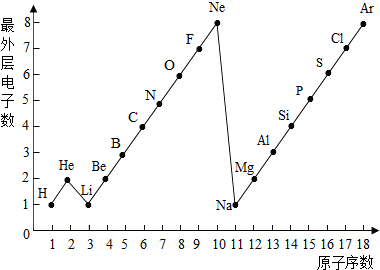 图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如右图.试回答:
图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如右图.试回答: