题目内容
【题目】t2℃时,将60.0g氯化钾和硝酸钾分别加入到各盛有100水的烧杯①和烧杯②中,充分搅拌后现象如图1所示,氯化钾和硝酸钾的溶解度曲线如图2所示。
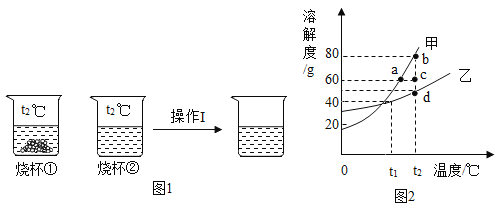
(1)t2℃时,溶解度大小关系为:氯化钾_____硝酸钾(选填:“>”、“<”或“=”)。
(2)烧杯②中的溶液是否达到饱和状态?_____(选填:“是”“否”或“无法判断”)。
(3)t1℃时,配制70.0g乙物质的饱和落液,需称量乙物质的质量_____g。
(4)由图1可推测氯化钾是图2中的_____物质(选填:“甲”或“乙”)。
(5)图1中操作Ⅰ前后的溶液状态变化过程可以在图2中表示为_____(填序号)。
A b点→a点 B c点→a点 C c点→b点 D c点→d点
【答案】< 否 20.0 乙 B
【解析】
t2℃时,将60.0g氯化钾和硝酸钾分别加入到各盛有100水的烧杯①和烧杯②中,烧杯①中有固体剩余,烧杯②中没有固体剩余,说明硝酸钾的溶解度大于氯化钾的溶解度。
(1)t2℃时,将60.0g氯化钾和硝酸钾分别加入到各盛有100水的烧杯①和烧杯②中,烧杯①中有固体剩余,烧杯②中没有固体剩余,说明硝酸钾的溶解度大于氯化钾的溶解度,故t2℃时,溶解度大小关系为:氯化钾<硝酸钾。
(2)t2℃时,将60.0g氯化钾和硝酸钾分别加入到各盛有100水的烧杯①和烧杯②中,烧杯①中有固体剩余,烧杯②中没有固体剩余,说明硝酸钾的溶解度曲线是甲曲线,由氯化钾和硝酸钾的溶解度曲线图可知,t2℃时,甲的溶解度为80g,故烧杯②中的溶液没有达到饱和状态。
(3)t1℃时,乙物质的溶解度为40g,配制70.0g乙物质的饱和落液,需称量乙物质的质量![]() 。
。
(4)t2℃时,将60.0g氯化钾和硝酸钾分别加入到各盛有100水的烧杯①和烧杯②中,烧杯①中有固体剩余,说明氯化钾的溶解度受温度的影响较小,故由图1可推测氯化钾是图2中的乙物质。
(5)图1中烧杯①中有固体剩余,烧杯②中没有固体剩余,经过操作Ⅰ后,烧杯①和烧杯②中均没有固体剩余,固体溶解,溶质的质量没有变化,烧杯①中溶液达到饱和状态,则图1中操作Ⅰ前后的溶液状态变化过程可以在图2中表示为c点→a点,故选B。

 一本好题口算题卡系列答案
一本好题口算题卡系列答案【题目】如图是工业上利用含SO2的烟气制备K2SO4的流程。
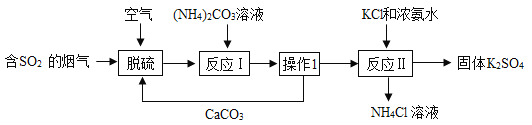
相关物质的溶解度如下表所示:
物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(1)石膏与饱和(NH4)2CO3溶液相混合,发生反应I时需不断搅拌,其目的是____________。
(2)“操作I”的名称是____________,实验室进行该操作时所用到的玻璃仪器有烧杯、玻璃棒、__________。
(3)你认为反应II在常温下能实现的原因是________________。
(4)NH4C1在农业上可以用作化肥,从NH4C1溶液中得到NH4C1晶体,可以采用加热浓缩、_______、过滤的方法。
(5)此工艺流程中可以循环利用的物质是_____________。