题目内容
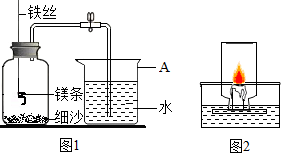 某学习小组用如图1进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某学习小组用如图1进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.(1)瓶底铺细沙的原因是
防止生成的熔融物溅落炸裂瓶底
防止生成的熔融物溅落炸裂瓶底
,燃烧、冷却后打开止水夹,水会进入集气瓶,还可以推断集气瓶中剩余气体的性质是剩余气体不能支持燃烧,不易溶于水
剩余气体不能支持燃烧,不易溶于水
.(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的
21
21
%.现进入集气瓶中水的体积约为其容积的70%,根据空气的组成推测原因可能是镁条与氮气能发生反应
镁条与氮气能发生反应
(3)小明同学由该实验得到启发,设计了如图2所示的测定实验:但是他看到的现象是水面并没有上升约
| 1 | 5 |
蜡烛燃烧消耗氧气但又生成新的气体
蜡烛燃烧消耗氧气但又生成新的气体
,由此我们总结出测定空气中氧气含量的反应物所满足的条件是反应物是固体且只和氧气反应,反应后不能生成气体物质
反应物是固体且只和氧气反应,反应后不能生成气体物质
.分析:(1)根据实验的注意事项和现象分析回答;
(2)根据空气中氧气的体积分数进行分析解答;
(3)根据蜡烛燃烧的生成物的状态分析解答.
(2)根据空气中氧气的体积分数进行分析解答;
(3)根据蜡烛燃烧的生成物的状态分析解答.
解答:解:(1)结合铁丝在氧气中燃烧的实验,瓶底铺一层细沙的目的是防止生成的熔融物溅落炸裂瓶底;最后剩余的气体不支持燃烧,也不溶于水.
(2)氧气约占空气体积的21%,氮气约占空气体积的78%,如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 21%.现进入集气瓶中水的体积约为其容积的70%,可能是镁条与氮气能发生反应;
(3)蜡烛燃烧消耗氧气,但生成物中有二氧化碳气体,故水面没有上升到理论位置,由此可总结出测定空气中氧气含量的反应物所满足的条件是:反应物是固体且只和氧气反应,且反应后不能生成气体.
故答案为:(1)防止生成的熔融物溅落炸裂瓶底;剩余气体不能支持燃烧,不易溶于水
(2)21、镁条与氮气能发生反应(或氮气与瓶内的其他物质反应而减少等)
(3)蜡烛燃烧消耗氧气但又生成新的气体;
反应物是固体且只和氧气反应,反应后不能生成气体.
(2)氧气约占空气体积的21%,氮气约占空气体积的78%,如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 21%.现进入集气瓶中水的体积约为其容积的70%,可能是镁条与氮气能发生反应;
(3)蜡烛燃烧消耗氧气,但生成物中有二氧化碳气体,故水面没有上升到理论位置,由此可总结出测定空气中氧气含量的反应物所满足的条件是:反应物是固体且只和氧气反应,且反应后不能生成气体.
故答案为:(1)防止生成的熔融物溅落炸裂瓶底;剩余气体不能支持燃烧,不易溶于水
(2)21、镁条与氮气能发生反应(或氮气与瓶内的其他物质反应而减少等)
(3)蜡烛燃烧消耗氧气但又生成新的气体;
反应物是固体且只和氧气反应,反应后不能生成气体.
点评:根据对空气组成成分的认识,利用镁的性质,分析导致实验中所出现现象的可能性;在平时的学习过程中要注意培养自己从题中资料获得信息解决问题的能力.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
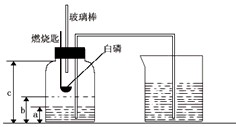 某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
①如图所示,连接仪器,检查装置的气密性.发现装置的气密性良好.
②在集气瓶里装进适量a 体积的水,燃烧匙里放一块白磷(其着火点是40℃),并在酒精灯上把玻璃棒下端加热,按图示装置把集气瓶中的空气密封起来,把长导管的另一端放入盛有足量水的烧杯中.(注:集气瓶内的长导管已伸到了瓶底)
③用力把预先加热过的玻璃棒按下与白磷接触,观察到白磷立即着火燃烧,产生大量白烟,同时放出大量的热.(注:白磷与红磷燃烧的产物相同)
④待白磷燃烧熄灭后,稍加振荡,白烟消失.
⑤待集气瓶完全冷却至室温,量出集气瓶中水的体积是b,整个集气瓶的体积是c.
⑥根据a、b、c三个数据,计算出空气中氧气的体积分数.
根据以上信息,回答下列问题.
(1)在白磷开始燃烧到最后熄灭的过程中,集气瓶内水面的变化情况是________.
(2)若实验非常成功,请写出a、b、c三个数据应满足的一个等式关系式:________.
(3)组内成员小葛为了证明实验完成后的集气瓶内是否还有氧气剩余,他没有利用其它的仪器和药品,仍是利用了上述实验涉及的仪器和药品,设计了一个实验,最后得出了瓶内一定没有氧气剩余的结论.你知道他是如何实验的吗?写出简要的实验步骤和实验现象.
| 实验步骤 | 实验现象 |
(5)组内成员小杭性格好动,无意间他发现向⑤步骤集气瓶内的水中滴加几滴紫色石蕊试液,水会变红.这一现象使组内成员积极地展开了讨论,成员小葛是由于二氧化碳溶于水,使溶液显酸性而导致的,但小明马上作出反对,原因是空气中二氧化碳的含量极少,而实验过程中又没有产生二氧化碳,短时间内不可能会使溶液显酸性.你认为谁的观点正确?________.若你认为小明的观点正确,那么请你对“变红”现象提出大胆地猜想:________.(若你认为小葛的观点正确,此空不填)
(6)在上述实验中,下列操作的实施和实验现象的出现,会导致实验最后产生的实际值大于理论值的是________
A.装置气密性不好 B.实验前集气瓶里没有装a 体积的水
C.集气瓶没有冷却到室温 D.用红磷代替白磷(红磷的着火点在240℃左右)
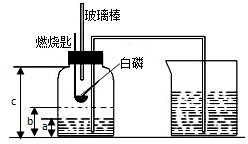 某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下: 化学实验是学习化学的基础,某兴趣小组同学在测定空气中氧气含量的实验中重新进行了探究:
化学实验是学习化学的基础,某兴趣小组同学在测定空气中氧气含量的实验中重新进行了探究: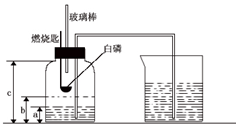 某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下: 化学实验是学习化学的基础,某兴趣小组同学在测定空气中氧气含量的实验中重新进行了探究:
化学实验是学习化学的基础,某兴趣小组同学在测定空气中氧气含量的实验中重新进行了探究: