题目内容
【题目】某纯碱样品中含有少量的氯化钠,现取24g该纯碱样品,加入100g水使其完全溶解,再加入158g氯化钙溶液,恰好完全反应后,过滤后得滤液262g(忽略实验过程中质量的损耗)。计算:
①纯碱样品中碳酸钠的质量;
②反应后所得溶液中溶质的质量分数为多少?(结果精确到0.1%)。
【答案】①21.2g②10.0%
【解析】
碳酸钙质量为:100g+24g+158g-262g=20g
解:设样品中碳酸钠的质量为x,生成氯化钠的质量为y。
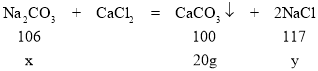
①碳酸钠的质量:
![]() x=21.2g
x=21.2g
②生成氯化钠的质量:
![]() y=23.4g
y=23.4g
原样品中氯化钠的质量:
24g-21.2g=2.8g
反应后溶液中溶质的质量分数为:
![]() ×100%=10.0%
×100%=10.0%
故填:21.2g;10.0%。

练习册系列答案
相关题目
【题目】为测定某CuSO4溶液中溶质的质量分数,取150g CuSO4溶液,平均分为三份,每份样品均按如图所示进行实验,实验数据见下表。请计算:
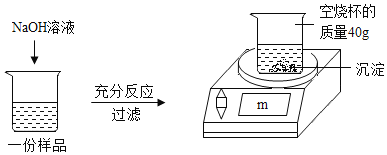
实验1 | 实验2 | 实验3 | |
样品质量/g | 50 | 50 | 50 |
NaOH溶液质量/g | 20 | 40 | 60 |
m/g | 42.45 | 44.9 | 44.9 |
(1)50g CuSO4溶液完全反应时,所得沉淀的质星为_____g。
(2)CuSO4溶液中溶质的质量分数为_____。