题目内容
实验室要从含少量铜粉的银(Ag)、锌混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属
随意编号为:A、B、C,并设计了如图流程:
(1)A、B、C三种金属的活动性顺序为 > > .
(2)金属A是 ,无色气体是 .操作a的名称是
(3)写出步骤①的反应的化学方程式: .
随意编号为:A、B、C,并设计了如图流程:

(1)A、B、C三种金属的活动性顺序为
(2)金属A是
(3)写出步骤①的反应的化学方程式:
考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:铜和银排在氢的后面,不能和稀硫酸反应,锌排在氢的前面,能和稀硫酸反应生成硫酸锌和氢气,因此A是锌;
铜比银活泼,能和硝酸银反应生成硝酸铜和银,因此C是银,则B是铜;
过滤可以把不溶于水的物质除去.
铜比银活泼,能和硝酸银反应生成硝酸铜和银,因此C是银,则B是铜;
过滤可以把不溶于水的物质除去.
解答:解:(1)A、B、C分别是锌、铜、银,活动性顺序是A>B>C.
故填:A;B;C.
(2)金属A是锌,无色气体是氢气,操作a的名称是过滤.
故填:锌;氢气;过滤.
(3)锌和稀硫酸反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
故填:Zn+H2SO4═ZnSO4+H2↑.
故填:A;B;C.
(2)金属A是锌,无色气体是氢气,操作a的名称是过滤.
故填:锌;氢气;过滤.
(3)锌和稀硫酸反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
故填:Zn+H2SO4═ZnSO4+H2↑.
点评:实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目


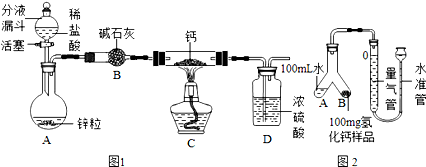
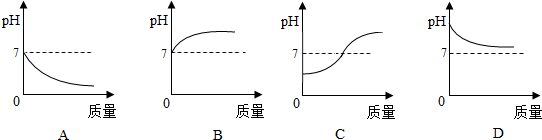
 (1)数字在化学式不同位置表示不同的意义:①表示微粒的数目 ②表示元素的化合价 ③表示离子的电荷数 ④表示每个分子中所含原子的个数请你判断下列化学式中的“2”分别表示上述哪种含义?(填序号)
(1)数字在化学式不同位置表示不同的意义:①表示微粒的数目 ②表示元素的化合价 ③表示离子的电荷数 ④表示每个分子中所含原子的个数请你判断下列化学式中的“2”分别表示上述哪种含义?(填序号)