题目内容
【题目】某兴趣小组准备通过锌与稀硫酸反应产生的氢气来测定稀硫酸中溶质的质量分数,装置如下:
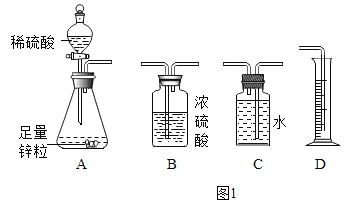

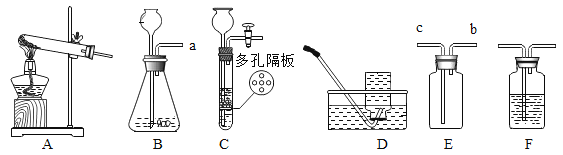
①小明同学用如图1所示装置进行实验,你认为他应该选择的最简易的装置及其连接顺序是:A→______→D。
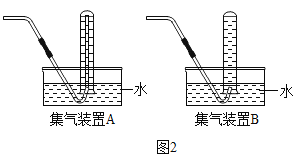
②小明若用图2装置收集氢气,应选择集气装置______(填“A”或“B”),为保证测量结果的准确性,收集气体的时机是______。
a导管口还没有气泡产生时
b导管口连续均匀冒出气泡时
c导管口冒出气泡很多时
③小张同学用如图3所示装置进行了实验:
Ⅰ下列能说明装置气密性良好的是______。
A连接仪器后,向水准管中注水,直至左右两边管内形成稳定高度差。
B向水准管内注水,连接好左侧装置,抬高水准管,左右两边液面始终相平。
Ⅱ反应完毕后,每间隔1分钟读取气体体积、气体体积逐渐减小,直至体积不变。气体体积逐渐减小的原因是______(排除仪器和实验操作的影响因素)。
Ⅲ若实验中测得稀硫酸的溶质质量分数偏大,下列可能的原因是______。
a装置漏气b读取数据时水准管的水面高于量气管的水面 c未待冷却就读取量气管读数
【答案】C B a A 反应放热、气体在冷却过程中体积逐渐减小 c
【解析】
解:①由题意可知,通过锌与稀硫酸反应产生的氢气来测定稀硫酸中溶质的质量分数,就要测出氢气的体积,小明同学用如图1所示装置进行实验,可用C装置收集氢气,排出水的体积就是氢气的体积,他应该选择的最简易的装置及其连接顺序是:A→C→D。
②小明若用图2装置收集氢气,氢气不溶于水,导气管伸入试管口即可,应选择集气装置是B,
为保证测量结果的准确性,收集气体的时机是:导管口还没有气泡产生时就伸入试管口,保证氢气全部被收集;故选:a;
Ⅰ.连接仪器后,向水准管中注水,直至左右两边管内形成稳定高度差,能说明装置气密性良好;故选:A;
Ⅱ.由于锌与稀硫酸反应能放出热量,气体的体积随温度的升高而增大,所以反应完毕后,每间隔1分钟读取气体体积、气体体积逐渐减小,直至体积不变。气体体积逐渐减小的原因是:反应放热、气体在冷却过程中,温度降低,体积逐渐减小。
Ⅲ.a.装置漏气,生成氢气的体积偏下,会使测定的结果偏小;
b.读取数据时水准管的水面高于量气管的水面,压强增大,读数的氢气的体积偏小,会使测定的结果偏小;
c.未待冷却就读取量气管读数,读数偏大,会使会使测定的结果偏大;
故选:c。

 阅读快车系列答案
阅读快车系列答案【题目】下表列出了硝酸钾在不同温度时的溶解度.
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
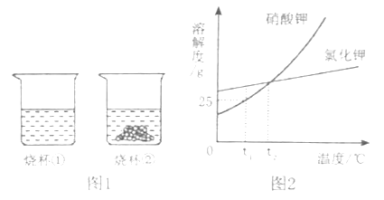
某兴趣小组做了以下实验:

(1)上述溶液中的溶剂是________,上述实验过程中得到的溶液一定属于不饱和溶液的是________(填数字序号),⑤所对应的实验现象是________.
(2)实验过程中,溶质的质量分数一定相等的是________(填数字序号).
(3)为了防止水体污染,小组同学提出了如下方案处理实验后的废液: 步骤I:将⑤继续冷却至0℃,过滤,共可回收得到KNO3固体________g.
步骤II:向滤液中加入________g水稀释,得到溶质的质量分数为1%的KNO3稀溶液,将此溶液做为化肥使用.
【题目】图一、图二是某兴趣小组探究金属、酸的化学性质时所做的两组实验。实验结束后,将两组实验试管中的物质分别全部倒入甲、乙两个洁净的烧杯中,据图回答:
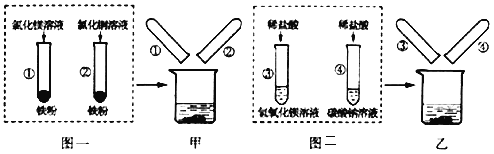
(1)在图一所示的实验中,试管②中发生反应的化学方程式是_____。
(2)甲烧杯中的物质完全反应后,发现红色固体物质明显增多。下列说法正确的是_____(填序号)
A.试管②反应后的固体中一定不含铁
B.完全反应后,甲烧杯中的固体一定含有铁
C.完全反应后,甲烧杯的溶液中可能含有Cu2+
D.完全反应后,甲烧杯的溶液中一定含有Mg2+、Fe2+
(3)乙烧杯中的物质充分反应后,仅观察到有白色沉淀,无其他现象。则试管④反应后的溶液中的溶质共有哪些_____(写化学式)。
(4)将乙烧杯内的物质进行过滤,对所得滤液中溶质成分进行了如下探究:
实验操作 | 实验现象 | 实验结论 |
步骤1:取少量滤液于试管中,向其中滴加足量硝酸钡溶液, | 有白色沉淀生成 | ①生成的白色沉淀是_____(写化学式,下同) ②滤液中的溶质共有哪些_____ |
步骤2:静置,向上层清夜中滴加无色酚酞试液 | 溶液变红 |
(5)在上述(4)的实验探究中,步骤1中加入足量硝酸钡溶液的目的是_____。
【题目】如表是国家对“饮酒驾车”和“醉酒驾车”的界定标准。
饮酒驾车 | 20mg/100mL≤血液中的酒精含量<80mg/100mL |
醉酒驾车 | 血液中的酒精合量≥80mg/100mL |
白酒、酒精和啤酒中均含有乙醇(俗称酒精,化学式为C2H5OH),饮酒后酒精可进入人体血液中。回答下列问题:
(1)乙醇分子中碳、氢、氧各原子个数比为_______,其中碳、氢元素的质量比是_______;
(2)乙醇中碳元素的质量分数为_______。(结果精确到0.1%)。
(3)饮酒会使人的神经系统过度兴奋或麻痹抑制,容易引发交通事故。某人饮酒后驾 车,被交警发现,经测定其每10mL血液中酒精含量为9.3mg,属于_______驾车。