题目内容
【题目】某校化学兴趣小组就空气中氧气的含量进行实验探究:

(进行实验)
(1)小组同学共同设计了如图1所示的装置,为了确保实验的成功,在装药品之前应该________,然后在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开弹簧夹。实验中集气瓶内红磷燃烧的文字表达式为_____。
(数据分析)实验结束后,整理数据如下:(注:集气瓶容积为100 mL)

(2)由表中数据,可知氧气约占空气体积的___ %(结果保留到小数点后一位)。
(实验反思)
(3)该实验能否将红磷换成铁丝,并说出理由:____________。
(4)通过本实验还可以推断实验结束后集气瓶中剩余主要气体的化学性质是____________。
(实验拓展)
(5)同学对实验进行反思后,提出了改进方法(图2所示),你认为改进后的优点是:_____
【答案】检查装置气密性 红磷+氧气![]() 五氧化二磷 20.3% 不能,这是因为铁丝不能在空气中燃烧,不能消耗氧气,实验后瓶内压强几乎不变,导致水不能进入集气瓶 既不燃烧也不支持燃烧 实验结果更准确,更环保
五氧化二磷 20.3% 不能,这是因为铁丝不能在空气中燃烧,不能消耗氧气,实验后瓶内压强几乎不变,导致水不能进入集气瓶 既不燃烧也不支持燃烧 实验结果更准确,更环保
【解析】
(1)测定空气中氧气含量的实验中,先要检查装置的气密性。红磷与氧气在点燃的条件下反应生成五氧化二磷,反应的文字表达式为:红磷+氧气![]() 五氧化二磷。
五氧化二磷。
(2)第2 组数据误差太大,故选1、3、4三组数据进行计算,故空气中氧气占(20+20+21)÷3÷100×100%=20.3%。
(3)铁不能在空气中剧烈燃烧,不能耗尽氧气,故该实验中不能将红磷换为铁。
(4)通过本实验还可以推断实验结束后集气瓶中剩余主要气体的化学性质是既不燃烧也不支持燃烧。
(5)改进后的装置的引燃是在集气瓶中进行的,这样改进后的优点是实验结果更准确,更环保。

【题目】某兴趣小组同学利用如图装置进行相关实验
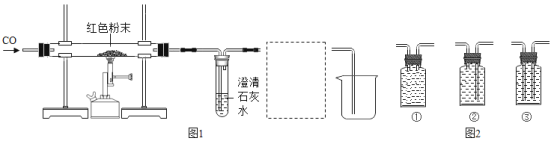
(实验1)模拟炼铁实验
(1)若样品为氧化铁,则A中的实验现象是___________,反应的化学方程式是_____,B中反应的化学方程式是_________。
(2)实验时要先通CO再加热的目的是___________。
(3)图1虚线框内的装置用于吸收CO2并收集CO,从图2(瓶内均为氢氧化钠溶液)中选择最合适的装置为___________(填序号)。
(实验2)测定样品的组成
若样品有氧化铁、氧化亚铁和四氧化三铁中的一种或几种组成,带充分反应后,实验数据记录如下:
样品质量 | 装置A中玻璃管和固体的总质量 | 装置B的质量 |
2.32g | 反应前55.72g | 反应前281.00g |
反应后55.08g | 反应后281.56g |
样品中铁元素和氧元素的质量比为____________。