题目内容
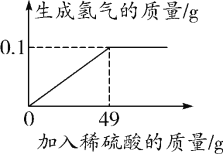
【题目】小王同学想测定某Cu-Zn合金中铜的质量分数,取合金粉末10 g,向其中逐渐加入一定溶质质量分数的稀硫酸,所加稀硫酸与生成氢气的质量关系如图所示。
请完成下列分析及计算:
(1)反应生成氢气的总质量为__g。
(2)计算合金中铜的质量分数。________
【答案】0.1 67.5%
【解析】
(1)根据图中的信息可知氢气的质量进行解答;
(2)利用锌与硫酸反应的化学方程式,根据氢气的质量求出锌的质量,进而求出铜的质量,进而求出黄铜中铜的质量分数进行解答。
解:(1)由图可知,完全反应后生成氢气的质量为0.1g;
(2)设该合金中锌的质量为x,
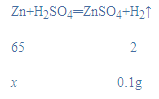
![]()
x=3.25g,
合金中铜的质量分数=![]() ×100%=65%;
×100%=65%;
答:合金中铜的质量分数为67.5%。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案【题目】空气、水、碳是生活中的重要物质。
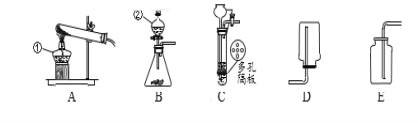
(1)关于如图所示实验,下列说法不正确的是____________
A.实验时红磷应足量
B.点燃红磷前先用弹簧夹夹紧乳胶管
C.红磷熄火后刻打开弹簧火
D.最终进入瓶中水的体积约为氧气的体积
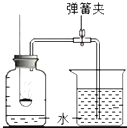
(2)自然界中的水都不是纯水,有些村庄取用地下水,可用__________区分地图1 空气中氧气含量的测定下水是软水还是硬水。在生活中,人们常用__________的方法来降低水的硬度。
(3)如图所示,与电源正极相连的玻璃管中生成的气体是__________,电解水化学方程式为____________,正极气体与负极气体的体积比是__________。
(4)根据下表提供的信息,填写有关含碳物质的对应特性。
物质用途 | 金刚石切割玻璃 | 石墨作电极 | 活性炭净水 |
对应特性 | ①_________________ | ②_________________ | ③_________________ |
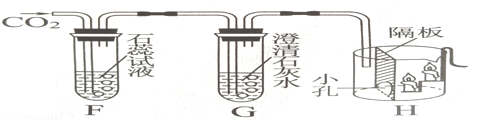
(5)液态二氧化碳灭火器可用于扑救档案室发生的火灾,下列说法正确的有_______
A.液态二氧化碳气化后不会污染档案资料
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳气化时吸热,降低了可燃物的着火点
(6)人类使用的化石燃料有煤、石油和天然气它们都属于__________(填“可再生”或”不可再“)能源。