题目内容
【题目】某环保小组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保小组的同学进行了以下实验。取废水500g,向其中加入溶质质量分数为20%的氢氧化钠溶液。测得沉淀质量与所加入的氢氧化钠溶液的质量关系如下图:
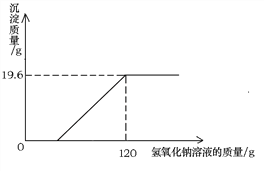
根据所得数据计算:
(1)500g该废水中硫酸铜的质量 _______________ 。
(2)该废水中硫酸的溶质质量分数_______________。
【答案】 32g 1.96%
【解析】(1). 解:设500g废水中CuSO4的质量为x,与CuSO4反应的NaOH溶液的质量为y,500g该废水中H2SO4的质量为z。
CuSO4+2NaOH==Cu(OH)2↓+Na2SO4
160 80 98
x y×20% 19.6g
![]() =
=![]()
![]() =
=![]()
x=32g y=80g
(2). H2SO4+2NaOH==Na2SO4+2H2O
98 80
Z ﹙120g-80g﹚×20%
![]() =
=![]()
z=9.8g
废水中硫酸的质量分数为∶![]() ×100%=1.96%.
×100%=1.96%.
答:500g该废水中CuSO4的质量是32g,该废水中硫酸的质量分数为1.96%
点睛∶本题是一道综合题,主要考查根据化学方程式并结合图表进行计算。

练习册系列答案
相关题目
【题目】下列对一些事实的解释中,不合理的是( )
选项 | 事 实 | 解 释 |
A | 将品红加入一杯清水中,清水很快变红 | 分子在不断运动 |
B | 氢气可用向下排空气法收集 | 相同条件下氢气密度比空气小 |
C | CO2和N2都能使燃着的木条熄灭 | CO2和N2一般都不支持燃烧 |
D | 25 m的氧气可以装入0.024 m的钢瓶中 | 氧分子的体积变小 |
A. A B. B C. C D. D