题目内容
【题目】下列图像不能正确反映其对应关系的是
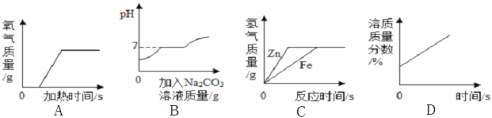
A.加热一定质量的高锰酸钾
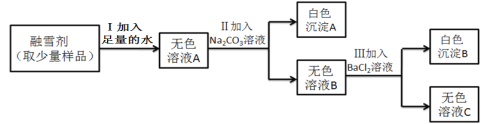
B.向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液
C.向等质量等质量分数的稀盐酸中分别加入过量的锌和铁
D.浓硫酸敞口放在空气中
【答案】D
【解析】
试题分析:加热一定质量的高锰酸钾,开始不会立刻反应,所以一段时间后才会产生气体,反应结束后气体就不会产生了,所以A正确; 向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液,开始氯化钙和碳酸钠反应生成碳酸钙和氯化钠,溶液的质量增大,会使得PH值增大,当盐酸和碳酸钠恰好反应完PH达到7,碳酸钠过量后溶液就会显示碱性;所以B正确;向等质量等质量分数的稀盐酸中分别加入过量的锌和铁,锌的活动性大于铁,所以锌会首先反应完,但是金属过量,因此得到的气体取决于酸,而酸的量相等,所以最后的气体的质量相等,所以C正确; D. 浓硫酸敞口放在空气中会吸水而质量分数会降低不会升高,故选D.

练习册系列答案
相关题目