��Ŀ����
����Ŀ��ʵ���Ҿ�����Ҫ��Ũ����ϡ�ͳ�ϡ���ᣬϡ�����ǻ�ѧ��Ӧ�ij��õ�ҩƷ��
��1��20��ʱ����ʵ������98%��Ũ��������20%��������Һ�� ����Ҫ����49g��������Ϊ20%���ᣬ����Ҫˮ������Ϊg��
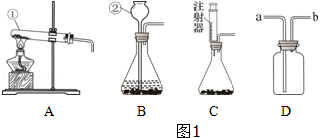
���õ��������У��ձ�����������������������ţ�
A��������ƽ��������У� B��ҩ�� C����ͷ�ι�
D.200mL��Ͳ E.50mL��Ͳ F.10mL��Ͳ
�۴��±����ҳ�ϡ������Ҫ�õ������ݣ�g/cm3 ��
������Һ���ܶȣ���λ��g/cm3��
��������/% | 10�� | 20�� | 30�� |
20% | 1.145 | 1.139 | 1.133 |
98% | 1.846 | 1.836 | 1.826 |
��2��Ϊ̽��98%��Ũ�����20%��ϡ��������ʲ��ijͬѧ��������ͼ1ʵ�飺 
��ͬѧ�۲�ʵ�����������Ũ����ϡ��������ʹ��ֽ̿����˵����ʹ��ͬ���ᣬ������ͬ�����ǵ����ʲ���ȫ��ͬ��
��3��ij��ѧѧϰС���о���������ʣ���20%������Һ�����Թ��У���ͼ2��ʾ��װ�����������ã��������Թ��м���ij���ʺ��¶ȼ��¶����ߣ��������� ��
A.�
B.����
C.ͭ��
D.�Ȼ���
E.�������ƣ�
���𰸡�
��1��39.2��CEF��1.836
��2��Ũ����Һ��Ũ�Ȼ����ʵ���������
��3��AE
���������⣺��1������Ҫ����49g��������Ϊ20%���ᣬ����Ҫˮ������Ϊ��49g��49g��20%=39.2g�� ���39.2�����õ��������У��ձ����������ͽ�ͷ�ιܡ�50mL��Ͳ��10mL��Ͳ����Ϊ��ȡˮ������ǣ�39.2g�£�1g/cm3��=39.2mL��50mL��Ͳֻ�ܹ���ȷ��1mL��10mL��Ͳ�ܹ���ȷ��0.1mL�������Ҫ50mL��Ͳ��10mL��Ͳ������Ͳ��
���CEF���ۼ�����Ҫ��Ũ��������ʱ����Ҫ֪��20��ʱŨ������ܶȣ�20��ʱŨ������ܶ���1.836g/cm3 ��
���1.836����2����ΪŨ���������ˮ�ԣ�����ܹ��۲쵽Ũ����ʹ��ֽ̿����˵����ʹ��ͬ���ᣬ������Һ��Ũ�Ȼ����ʵ�����������ͬ�����ǵ����ʲ���ȫ��ͬ��
���Ũ����Һ��Ũ�Ȼ����ʵ�������������3�����Թ��м���ij���ʺ��¶ȼ��¶����ߣ�˵����������ʺ�ϡ�����Ϻ���ȣ�п��ϡ���ᷴӦ��������п��������ͬʱ���ȣ��������ƺ�ϡ���ᷴӦ���������ƺ�ˮ��ͬʱ���ȣ���˼�������ʿ�����п�����������ƣ�
��ѡ��AE��
�����㾫����������Ҫ�������ܽ�ʱ�����Ȼ������������֪ʶ�㣬��Ҫ�����ܽ�ʱ���ȡ���������<�ܽ����ȣ���NH4NO3�ܽ⣻�ܽ���ȣ���NaOH�ܽ⡢ŨH2SO4�ܽ⣻��û��������������NaCl>������ȷ�����⣮