题目内容
【题目】甲、乙两物质的溶解度曲线如右图所示,下列说法正确的是( )
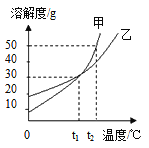
A. t1℃时,甲和乙的溶解度相等
B. 甲和乙的饱和溶液,从t1℃升温到t2℃,仍是饱和溶液
C. t2℃时,在100g水中放入60g甲,形成不饱和溶液
D. t1℃时,甲和乙各30g分别加入80g水中,均能完全溶解
【答案】A
【解析】A.在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。t1℃时,甲和乙的溶解度曲线交于一点,所以t1℃时,甲和乙的溶解度相等;B. 从图中信息可知,甲和乙的溶解度都随温度的升高而增大,所以甲和乙的饱和溶液,从t1℃升温到t2℃,得到是不饱和溶液;C. t2℃时,甲的溶解度为50g,在100g水中放入60g甲,只能溶解50g甲,形成饱和溶液,剩余固体甲10g; D. t1℃时,甲和乙溶解度为30g,即t1℃时,各100g溶剂里达到饱和时,所溶解的溶质的质量。所以30g分别加入80g水中,都不能完全溶解。选A

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目