题目内容
【题目】右图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中不正确的是
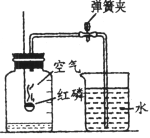
A.集气瓶内加入少量水可吸收生成的五氧化二磷
B.该实验所用红磷的量不足可能造成气体减少的体积小于五分之一
C.实验时,点燃的红磷要立即伸入集气瓶中,并塞紧橡胶塞
D.红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹
【答案】D
【解析】
试题分析:A、五氧化二磷会溶于水,故集气瓶内加入少量水可吸收生成的五氧化二磷,正确,B、该实验所用红磷的量不足,就不能充分消耗瓶内的氧气,可能造成气体减少的体积小于五分之一,正确,C、实验时,点燃的红磷要立即伸入集气瓶中,并塞紧橡胶塞,防止由于受热膨胀瓶内的气体排出,使测量结果偏大,正确,D、红磷燃烧产生大量的白烟,而不是白雾,火焰熄灭后不能立刻打开弹簧夹,因为此时瓶内气体还处于膨胀状态,错误,故选D

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案【题目】(14分)利用下列所示仪器、药品(及其它必要物品)设计制取氧气和试验其性质的实验对比方案。
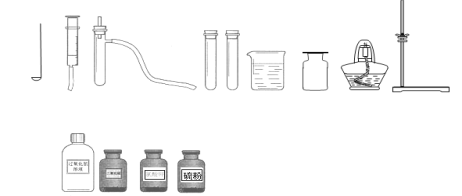
(1)对比加入试剂顺序对于制取氧气反应速率的影响
方法一:把二氧化锰加入装有过氧化氢溶液的试管中
| 方法二:把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中
|
现象:方法一中,立即产生大量的气泡,一会儿,产生气泡的速度越来越慢; 方法二中,持续并均匀地产生气泡; | |
结论:方法__①____可以得到平稳的氧气流。通过对比实验可知,对于固体和液体反应制取气体时,加入试剂的顺序对反应速率有影响,若想得到平稳的气流,应该先加___②____,(填“固体”或“液体”,下同)然后再缓缓加入 _____③_____ | |
(2)对比不同反应物制取氧气的反应速率
反应物药品的名称 | 反应的文字表达式 | 填选用制取和收集装置的仪器名称 |
方法一:过氧化氢溶液、二氧化锰 | ①_____________________ | 试管(带支管)、注射器、__②____ |
方法二:氯酸钾、二氧化锰 | ③___________________ | 此空不用填 |
结论:对比两种制取氧气的方法,方法一更简单。因为同样在二氧化锰的催化剂下,该方法制取氧气反应迅速,______ ④ _________。 | ||
(3)对比硫在空气里与在氧气中燃烧的现象
实验名称 | 操作步骤 | 实验现象 |
硫在空气里燃烧 | 取少量的硫粉于燃烧匙中,把燃烧匙放置在外焰上加热至硫粉燃烧起来,观察现象 | ①_____________________ |
硫在氧气中燃烧 | ②_____________________ | 在氧气中燃烧更剧烈,发出_____③____火焰,放热,生成有刺激性气味的气体 |
结论:条件(如浓度、温度)对化学反应是有影响的。硫在空气中燃烧不如在氧气中燃烧剧烈,是因为空气中_________④_________相对较少。 | ||
