题目内容
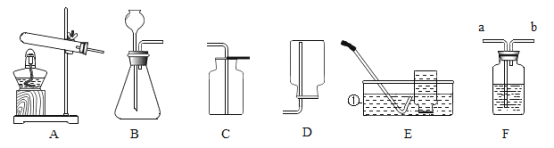
【题目】实验室配制100g溶质质量分数为5%的氯化钠溶液。实验操作如下:
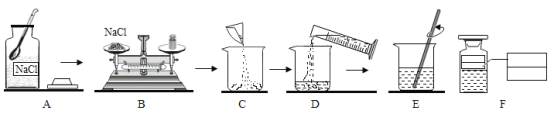
(1)需称量氯化钠的质量是_____g。
(2)操作D中量筒的量程是_____(填“10mL”、“50mL”或“100mL”)。
(3)E中玻璃棒的作用是_____。
(4)配制好的溶液要装在试剂瓶中,并贴好标签。请在标签中填上相应的内容。_____
【答案】5 100mL 加速溶解 NaCl溶液 5%
【解析】
(1)根据溶质质量=溶液质量×溶质质量分数进行分析;
(2)量筒量程的选择遵循“大而近”原则,据此分析。
(1)实验室配制100g溶质质量分数为5%的氯化钠溶液,该溶液的溶液质量为100g,则溶质质量=100g×5%=5g,因此需称量氯化钠的质量为5g;
(2)因为溶液质量为100g,溶质质量为5g,则溶剂质量=100g-5g=95g,95g水的体积约为95mL,因此操作D中量筒的量程为100Ml;
(3)E中玻璃棒的作用是搅拌,以加速溶解;
(4)该溶液为浓度为5%的NaCl溶液,因此标签上需注明溶液名称和浓度。

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目