题目内容
【题目】如图为空气成分示意图(按体积计算),下列说法错误的是
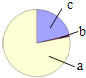
A. a气体表示氮气、氮气的体积分数约占空气的78%
B. c气体可以供给动植物呼吸
C. CO2、NO2、SO2是污染空气的三种有毒气体
D. 通常情况下,空气各成分的含量相对稳定
【答案】C
【解析】空气的成分及各成分的体积分数分别是:氮气占78%、氧气占21%、稀有气体占0.94%、二氧化碳占0.03%、其它气体和杂质占0.03%;
A.由图可知,a占的体积分数最大,是氮气,故正确;
B.由图可知,c为氧气,故c气体可以供给动植物呼吸,故正确;
C.二氧化碳是空气的成分之一,无毒,不属于空气污染物,错误;
D.空气中各成分的含量相对稳定,不同的地区,不同的年份略有差异,故正确。

 阅读快车系列答案
阅读快车系列答案【题目】研究盐类物质的性质时,甲、乙、丙三位同学分别向NaHCO3溶液中滴加石灰水,均产生白色沉淀.他们分别设计实验方案,对自己过滤后的滤液中溶质的成分进行如下探究.一、定性研究
【实验准备】用一定溶质的质量分数的NaHCO3溶液、NaOH溶液和Na2CO3溶液进行如下实验,为设计实验方案提供参考.
NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
加入酚酞溶液 | 溶液变红 | 现象Ⅰ | 溶液变红 |
加入CuSO4溶液 | 产生气泡和蓝色沉淀 | 现象Ⅱ | 产生气泡和蓝色沉淀 |
加入CaCl2溶液 | 无明显变化 | 无明显变化 | 产生白色沉淀 |
加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 | 澄清石灰水无明显变化 |
表中的现象Ⅰ为__________;现象Ⅱ为产生蓝色沉淀,对应反应的化学方程式是_________________________。
【查阅资料】
(1)氯化钙溶液显中性.
(2)滤液中所含的溶质有以下几种可能:①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④Na2CO3和NaHCO3;⑤Na2CO3和NaOH
【实验及分析】甲同学:取少量滤液于试管中,滴加过量的稀盐酸,产生大量无色气泡,则滤液中的溶质是Na2CO3.乙同学:取少量滤液于试管中,向其中通入少量CO2,产生白色沉淀,则滤液中的溶质是NaOH和Ca(OH)2.丙同学:分别取少量滤液于两支试管中,向一支试管中滴加CaCl2溶液,有白色沉淀产生;将另一支试管中的滤液加热至沸腾,将产生的气体通入澄清石灰水,澄清石灰水变浑浊,则滤液中的溶质是Na2CO3和NaHCO3.
【反思与评价】
(1)老师认为乙、丙同学的实验方案和结论合理.
①丙同学的实验中,加入CaCl2溶液的目的是__________________。
②根据乙同学的结论,NaHCO3溶液与澄清石灰水反应的化学方程式是_________。
(2)老师认为甲同学的实验方案和结论存在不足.丁同学通过以下实验帮助甲同学确认了滤液中溶质的成分.
实验操作 | 实验现象 | 实验结论 |
取少量滤液于试管中,加入过量的__________的溶液 | 有白色沉淀生成 | 滤液中的溶质是Na2CO3和NaOH |
过滤,向滤液中滴加______溶液 | _____________________ |
(3)结合此次探究活动,你认为下列说法正确的是_________(填字母序号)。
a.盐溶液可能显碱性
b.化学反应的产物与反应物的量有关
c.碱和盐反应一定生成另外一种碱和另外一种盐
d.判断溶液混合后的成分不仅要考虑产物,还要考虑反应物是否过量。
二、定量分析
已知碳酸钠稳定而碳酸氢钠(NaHCO3)不稳定,碳酸氢钠受热易分解,反应的化学方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O有NaHCO3和Na2CO3混合物13.7g,将其充分加热至固体质量不再减少,得剩余固体.将产生的气体通入足量的Ca(OH)2溶液中,产生5.0g沉淀.如果将剩余固体溶于足量的稀盐酸,会产生多少克CO2 ?____________
Na2CO3+CO2↑+H2O有NaHCO3和Na2CO3混合物13.7g,将其充分加热至固体质量不再减少,得剩余固体.将产生的气体通入足量的Ca(OH)2溶液中,产生5.0g沉淀.如果将剩余固体溶于足量的稀盐酸,会产生多少克CO2 ?____________