题目内容
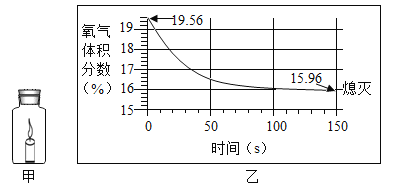
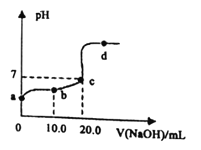
【题目】利用数字化实验可以更准确地比较不同状态的碳酸钙与稀盐酸反应的速率。如图所示,倾斜锥形瓶使试管内稀盐酸流入瓶中与固体发生反应,瓶内气压的变化如曲线所示。下列有关说法正确的是:
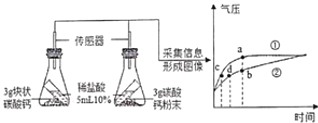
A. 曲线①表示的是块状碳酸钠与稀盐酸的反应
B. b点表示碳酸钙与盐酸反应已停止
C. 等质量不同状态的碳酸钙参加反应,粉末状碳酸钙产生CO2质量更多
D. 对比曲线①②中c、d两点可知,产生相同质量的二氧化碳,粉末状碳酸钙用时更少
【答案】D
【解析】
A、粉末状碳酸钙和稀盐酸反应速率快,反应需要时间短,曲线①表示的是粉末状碳酸钙与稀盐酸的反应,故A错误;
B、b点时二氧化碳的质量不断增大,表示碳酸钙与盐酸反应正在进行,故B错误;
C、等质量不同状态的碳酸钙参加反应,粉末状碳酸钙产生CO2速度较快,但产生的二氧化碳质量相等,故C错误;
D、曲线①表示的是粉末状碳酸钙与稀盐酸的反应,对比曲线①②中c、d两点可知,产生相同质量的二氧化碳,粉末状碳酸钙用吋更少,故D正确。故选D。

 名校通行证有效作业系列答案
名校通行证有效作业系列答案【题目】为了探究金属活动性,将锌和铜分别放入稀硫酸中,铜不反应而锌的表面有气泡产生,写出锌和稀硫酸反应的化学方程式:______。
老师告诉学生,铜和浓硫酸在加热的条件下也能反应且产生气体。
(提出问题)铜与浓硫酸反应的生成物是什么?其中气体是什么?
猜想假设)同学们对产生的气体作出了猜想。
猜想一:氢气;猜想二:二氧化硫;猜想三:氢气和二氧化硫的混合物。
(查阅资料)二氧化硫可以使品红溶液褪色,也能被氢氧化钾溶液吸收。浓硫酸只吸收水。
(实验探究)师生设计了如下装置进行实验![]() 部分仪器省略
部分仪器省略![]() ,请完成下列表格。
,请完成下列表格。
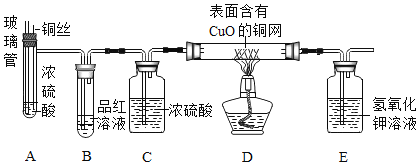
主要实验步骤 | 主要现象 | 解释或结论 |
①加热装置A一段时间 | 装置B中的现象是 ______ | 有二氧化硫生成 |
②点燃装置D处酒精灯 | 装置D玻璃管中无明显现象 | 猜想 ______ 正确 |
③停止加热,将铜丝上提,向装置A中玻璃管鼓入空气 | | |
④冷却,将A中液体用水稀释 | A中液体变为 ______ 色 | 有硫酸铜生成 |
(表达交流)(1)在步骤③中,鼓入空气的目的是______。
(反思拓展)(2)若将装置A中铜丝换成锌片,随着反应的进行,硫酸的浓度逐渐变小,装置D玻璃管中看到的现象是______,C装置的作用是:______。
(3)下列各组药品能够证明锌的活动性比铜强的是______![]() 填序号
填序号![]() 。
。
①锌、铜、稀盐酸
②锌、硫酸铜溶液
③锌、铜、氯化镁溶液
(1)加热A装置一段时间后,气泡产生的速率由快变慢最后不再产生,请对这一现象进行解释:______。
(2)请尝试写出铜与浓硫酸反应的化学方程式:______。